
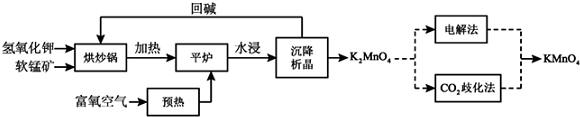
���� ��һ��̼��Ƶ��Ʊ�
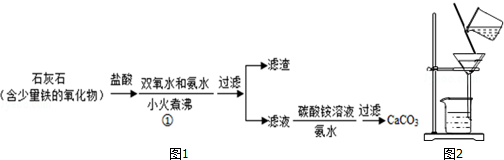
�����̿�֪�������ᣬ̼��ơ�������������ܽ⣬��˫��ˮ�������������ӣ��Ӱ�ˮ��������ת��Ϊ���������˺����Һ�к����ᣬ�Ӱ�ˮ�к��ᣬ���õõ�̼��Ƴ�����
��1������к��ᣬС��������ڳ������ɣ�
��2��������ѭһ�������������ݴ˷���ѡ�
�������������Ƶ��Ʊ�
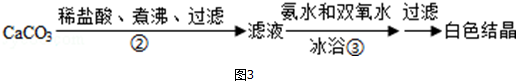
��3�������̿�֪��̼����������������Һ���д����������壬��Һ���ܽ������̼����ʱ��Һ�����ԣ�����Һ��е������Ǹϳ��ܽ�Ķ�����̼��
��4���¶ȹ��߹��������ҷ����ֽ⣮
��� �⣺��һ��̼��Ƶ��Ʊ�
�����̿�֪�������ᣬ̼��ơ�������������ܽ⣬��˫��ˮ�������������ӣ��Ӱ�ˮ��������ת��Ϊ���������˺����Һ�к����ᣬ�Ӱ�ˮ�к��ᣬ���õõ�̼��Ƴ�����
��1������ټ��백ˮ��Ŀ�����кͶ�������ᣬ���������ӣ�С����е�������ʹ�����������������ڹ��ˣ�
�ʴ�Ϊ�����˷��룻
��2��a��©��ĩ�˾���δ�����ձ��ڣ�Ӧ©��ĩ�˾�������ձ��ڣ���a����
b������������������ʹҺ��˳�����£���b��ȷ��
c������ֽʪ��ʹ�����©���ڣ���ֹҺ�����ֽ��©���ķ�϶���£���c��ȷ��
d����ֽ��ԵӦ����©���ϱ�Ե����d����
e��������������©������������Լӹ������ٶȣ����ܵ�����ֽ������ʧ�ܣ���e����
�ʴ�Ϊ��ade��
�������������Ƶ��Ʊ�
�����̿�֪��̼����������������Һ���д����������壬���˺���Һ���Ȼ��ơ���ˮ���������ⷴӦ����CaO2��NH4Cl��ˮ���ٹ��ˣ�ϴ�ӵõ��������ƣ�
��3������ڵľ������Ϊ��μ���ϡ���ᣬ����Һ���д����������壬��Һ���ܽ������̼����ʱ��Һ�����ԣ�����Һ��У����ȹ��ˣ�����Һ��е������dz�ȥ��Һ���ܽ�Ķ�����̼��
�ʴ�Ϊ�����ȥ��Һ���ܽ�Ķ�����̼��
��4��������з�Ӧ�Ļ�ѧ����ʽΪCaCl2+2NH3��H2O+H2O2=CaO2+2NH4Cl+2H2O���÷�Ӧ��Ҫ�ڱ�ԡ�½��У�ԭ�����¶ȹ���ʱ˫��ˮ�ֽ⣬
�ʴ�Ϊ���¶ȹ���ʱ˫��ˮ�ֽ⣮
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ�鼼�ܡ����ʵ�����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע�����ʵ����ʼ�Ӧ�ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
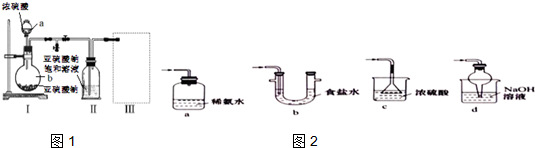
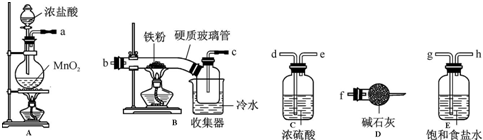
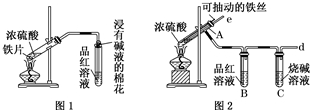 ijУ��ѧ��ȤС��Ϊ̽������Ũ���ᷴӦ�������ͼ1��ͼ2��ʾװ�ý���ʵ�飮
ijУ��ѧ��ȤС��Ϊ̽������Ũ���ᷴӦ�������ͼ1��ͼ2��ʾװ�ý���ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
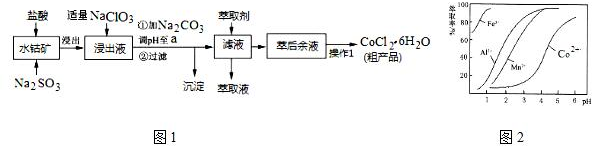
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
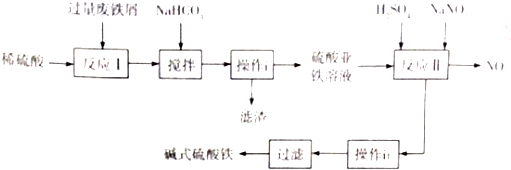
| ������ | Fe��OH��3 | Fe��OH��3 | Al��OH��3 |
| ��ʼ������pH | 2.3 | 7.5 | 3.4 |
| ��ȫ������pH | 3.2 | 9.7 | 4.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | c���Ӧ����Һ�д������ڵ����ӿ���Ϊ��Na+��H+��Cl-��NO3- | |
| B�� | ��25��ʱ��KCl��Һ���ȵ�t�棬�����Һ�е�c��OH-����a��仯��b�� | |
| C�� | t�棼25�� | |
| D�� | ac���ϵ�����һ����Һ����c��H+��=c��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com