
��֪��3 mol NaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ���������жϲ���ȷ����
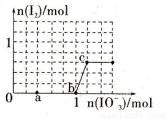
A����ԭ�ԣ�HSO3��>I���������ԣ�IO3��>I2>SO42��
B��a�㴦������������SO42������ԭ������I��
C������Һ�е�I��Ϊ0.4 molʱ�������KIO3һ��Ϊ0.4 mol
D������KIO3��Һ�еμ�NaHSO3��Һ����Ӧ��ʼʱ�����ӷ���ʽΪ��2IO3��+5HSO3��=I2+5SO42��+3H++H2O
 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ������ѧ��������8.28����ѧ�Ծ��������棩 ���ͣ�ѡ����
��nAΪ�����ӵ���������ֵ������˵����ȷ����
A�������£�46g NO2��N2O4����2nA����ԭ��
B��1mol Na�ڿ�����ȼ�գ�ת��2nA������
C��1L0.1mol��L��1CH3COOH��Һ�к���0.1nA��H+
D������£�22.4LHF�к���nA��HF����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶��Ͽ�ѧ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���ȼ�ϵ�˵��������ǣ� ��
A��ȼ��ȼ�ղ���CO2����������֮һ
B����ʯȼ����ȫȼ�ղ�����ɴ�����Ⱦ
C����Һ��ʯ��������ȼ�Ϳɼ��ٴ�����Ⱦ
D��ȼ�ϲ���ȫȼ���ŷŵ�CO�Ǵ�����Ⱦ��֮һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ��һ�Ͽ�ѧ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͭ��ұ�������������·�Ӧ������5FeS2+14CuSO4+12H2O=7Cu2S+5FeSO4+12H2SO4�����ڴ˷�Ӧ������˵����ȷ���ǣ���
A��Cu2S��������������ǻ�ԭ����
B��5 mol FeS2������Ӧ����10mol����ת��
C�������е�SO42-��һ��������������
D��FeS2ֻ����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������һ�и�����ѧ�ڿ�ѧ�����ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
������I(C12H14O3)���Ʊ�Һ�����ϵ��м���֮һ��������к���ȩ����������I������E��H��һ�������ºϳɣ�
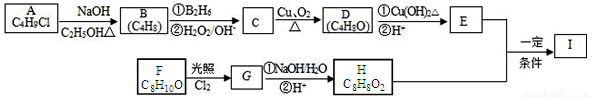
��֪������Ϣ���� A�ĺ˴Ź������ױ�����ֻ��һ�ֻ�ѧ�������⣻
��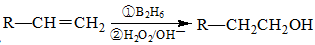
�ۻ�����F�����ϵ�һ�ȴ���ֻ����������Fe3+����ɫ��
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ���
��ش��������⣺
��1��A�Ľṹ��ʽΪ ��B���������ŵ�������
��2��C������Ϊ ��E�ķ���ʽΪ ��
��3��A��B��C��D�ķ�Ӧ���ͷֱ�Ϊ �� ��
��4��д��G��H�з�Ӧ�ٵĻ�ѧ����ʽ ��
��5��I�Ľṹ��ʽΪ ��
��6��I��ͬϵ��J��I����Է�������С28��J��ͬ���칹������ͬʱ���������������ٱ�����ֻ������ȡ�������ڼ��ܷ���������Ӧ�������뱥��NaHCO3��Һ��Ӧ�ų�CO2������ ��(�����������칹)��J��һ��ͬ���칹�巢��������Ӧ���ữ��˴Ź�������Ϊ����壬�ҷ������Ϊ2��2��1��д��J������ͬ���칹��Ľṹ��ʽ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������һ�и�����ѧ�ڿ�ѧ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ����٤������������������ȷ����
A��7.8 g Na2O2��������������0.2NA
B��0.1 mol 16OD�� ���Ӻ��еĵ��ӡ���������Ϊ1.0NA
C�����³�ѹ�£�42g��ϩ�Ͷ�ϩ��������У����Լ���Ϊ 6 NA
D���ܱ�������2 mol NO��1 mol O2��ַ�Ӧ������ķ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ����У������ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A�������ȼ����Ϊ��H��-890.3 kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ��H��-890.3 kJ��mol-1
B����֪H+(aq)+OH-(aq)== H2O(l) ��H��-57.3 kJ��mol-1����ϡH2SO4��Һ��ϡBa(OH)2 ��Һ��Ӧ�ķ�Ӧ�Ȧ�H ==2��(-57.3) kJ��mol-1
C��Mg��CO2��ȼ������MgO��C���÷�Ӧ�л�ѧ��ȫ��ת��Ϊ����
D�������£���ӦC(s)+CO2(g)===2CO(g)�����Է����У���÷�Ӧ�Ħ�H > 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶���9�µ��л�ѧ�Ծ��������棩 ���ͣ��ƶ���
�ס��ҡ���Ϊ�������ʡ�A��B��C��D��E��F��G��H��Ϊ��ѧ��ѧ�г����Ļ��������B��G����ɫ��Ӧ��Ϊ��ɫ��C��ʹƷ����Һ��ɫ����һ�������£��������ת����ϵ��ͼ��ʾ��
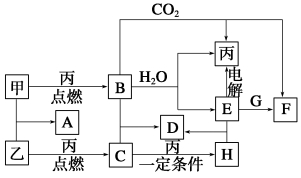
��ش��������⣺
��1���û�ѧʽ��ʾ����Ϊ__________��HΪ__________��
��2��A�ĵ���ʽΪ___________________��
��3�����E��ˮ��Һʱ��E��������_____________________
��4��д��B��C�D��D�Ļ�ѧ����ʽ__________________________
д��E��G�D��F�����ӷ���ʽ_______________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ��һ�Ͽ�ѧ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��������������ȫȼ������8.8g������̼��5.4gˮ��������������ʵ����������ȷ����( )
A. ������ֻ����̼Ԫ�غ���Ԫ��
B. ��������̼Ԫ������Ԫ�ص�������Ϊ12 : l
C. ������һ������̼Ԫ�غ���Ԫ�أ����ܺ�����Ԫ��
D. �����ʵķ�����̼ԭ�Ӻ���ԭ�ӵĸ�����Ϊ1 : 2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com