
����Ŀ���й��ڶ��������Ժ������ü�ӵ绯ѧ���Դ�����Ⱦ�� NO ����������������ԭ��ʾ����ͼ(����Ĥ����H+�� H2O ͨ��)����������ж���ȷ����

A.�缫��Ϊ�������缫��ӦʽΪ 2H2O+2e- =2OH- +H2��
B.���������Ӵӵ缫����缫���������ƶ�
C.�������еķ�ӦΪ 2NO+ 2S2O42-+H2O=N2+4HSO3-
D.ÿ����1molNO������������16g
���𰸡�C
��������
�ڵ缫��HSO3-ת��ΪS2O42-��SԪ�ػ��ϼ���+4�۽���Ϊ+3�۷�����ԭ��Ӧ����õ缫�����ص��������缫��Ϊ���ص��������ڵ缫����H2Oʧ���ӷ���������Ӧ����O2��H+��
A���缫��Ϊ���ص��������缫��ӦʽΪ2HSO3-+2e-+2H+ = S2O42-+2H2O��A����ȷ��
B����������������H+������������H+�����������Ӵӵ缫����缫���������ƶ���B����ȷ��
C���Ӽ�ͷ��ָ��ȷ����������S2O42-��NO��Ӧ������HSO3-��N2��������ӦΪ 2NO+ 2S2O32-+H2O=N2+4HSO3-��C��ȷ��
D��ÿ����1molNO������2HSO3-�� S2O42-����������34g������H2O��![]() O2����������16g��������������34g-16g=18g��D����ȷ��
O2����������16g��������������34g-16g=18g��D����ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����֣���![]() ��ѹ�ϳɼ״���Ӧ��
��ѹ�ϳɼ״���Ӧ��![]() )�У�
)�У�![]() �����︺�ص�
�����︺�ص�![]() �������������Ӵ������и��ԣ���ʾ�����õ�Ӧ��ǰ�����ش��������⣺
�������������Ӵ������и��ԣ���ʾ�����õ�Ӧ��ǰ�����ش��������⣺
��1��![]() ��
��![]() ������
������![]() ԭ�ӵ��ӻ���ʽ�ֱ�Ϊ__________��__________��
ԭ�ӵ��ӻ���ʽ�ֱ�Ϊ__________��__________��
��2����![]() ��ѹ�ϳɼ״���Ӧ���漰��4�������У��е�Ӹߵ��͵�˳��Ϊ____��ԭ����_____��
��ѹ�ϳɼ״���Ӧ���漰��4�������У��е�Ӹߵ��͵�˳��Ϊ____��ԭ����_____��
��3�����������Ʊ�������Ӧ������ԭ�ϣ�![]() �еĻ�ѧ������
�еĻ�ѧ������![]() ���⣬������__________��
���⣬������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�����ҵ�Ͷ�������ڽ������������ǧ��������Һ����ش���ʾ����վ��������Һ������ܷ�ӦΪFe2+ + Cr3+![]() Fe3 + + Cr2+������ʾ��ͼ��ͼ������˵���������
Fe3 + + Cr2+������ʾ��ͼ��ͼ������˵���������
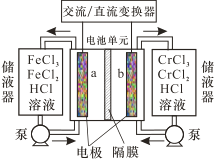
A.�ŵ�ʱa�缫��ӦΪ Fe 3++e- =Fe2+
B.���ʱb�缫��ӦΪ Cr3++e- =Cr2+
C.�ŵ������H+ͨ����Ĥ��������������
D.�õ���ޱ�ը���ܣ���ȫ�Ըߣ����Ժ�ʴ����Խϵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯���������ǵ��ճ���������ͻ�����ҵ���������������������ش���������:
��1��������ũҵ���Ϻͻ�����������Ҫԭ�ϣ������ʽΪ____��
��2����������(NaN3)��ҩ���Ʊ����ϳ�Ӱ��ѧ�����������������ҵ���Ź㷺����;���������ʼ��ױ�ը�����и���������NaClO��Һ�Ժ��е������Ƶ���Һ���д���������һ������Ⱦ�����嵥�ʣ���Ӧ�Ļ�ѧ����ʽΪ______________��
��3�����̵�����ũҵ��ѧ���о����������⡣��ij�������������������N2��ˮ��Ӧ������NH3��
��֪:
��i��4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) ��H1=-1266 kJ/mol��
2N2(g) +6H2O(g) ��H1=-1266 kJ/mol��
��ii��H2O(g)=H2O(l) ��H2= -44.0kJ/mol��
��2N2(g) +6H2O(l)![]() 4NH3(g)+3O2(g) ��H3=______kJ/mol��
4NH3(g)+3O2(g) ��H3=______kJ/mol��
��4��Ŀǰ���˹��̵�����ɹ���Ӧ�þ��ǹ�ҵ�ϳɰ�:
N2(g) +3H2(g)![]() 2NH3(g) ��H=-92.4kJ/mol����1.00molN2��3.00molH2���뵽�ݻ�Ϊ3L�ĺ����ܱ������У�����������Ӧ��
2NH3(g) ��H=-92.4kJ/mol����1.00molN2��3.00molH2���뵽�ݻ�Ϊ3L�ĺ����ܱ������У�����������Ӧ��
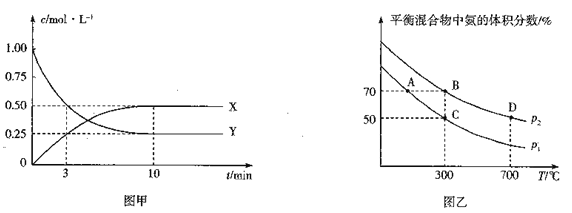
��ͼ���Dz��X��Y ��Ũ����ʱ��仯������.����Y Ϊ_____(д��ѧʽ)����Ӧ�ﵽƽ��ʱ��ƽ����Ӧ����v(N2) =_________��
���ڲ�ͬ�¶Ⱥ�ѹǿ�£�ƽ����ϵ��NH3������������¶ȡ�ѹǿ��ϵ��ͼ������ѹǿp1_____p2(����>����<����=��������ȷ��������ͬ)��B��D �����ƽ�ⳣ��KB____KD��B ��N2 ��ת����=_________(����3λ��Ч����)��
��5������ˮ��ɽ���ǽ�ɽ��ɽ��������ԭ���ԭ��(6NO2 +8NH3=7N2+12H2O)���Դ��������������NH3 β��,װ��ԭ��ͼ��ͼ��:
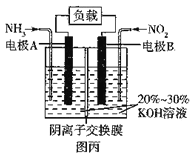
������ӦʽΪ__________�����б�״����4.48 L NO2������ʱ��ת�Ƶ��ӵ����ʵ���Ϊ_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѱ�(TiO2)����Ҫ�İ�ɫ������LiFePO4������ӵ�ص��������ϡ�һ������������( ��Ҫ�ɷ�ΪFeTiO3 ������Fe2O3 )�����Ѱۺ�LiFePO4 ������������������ͼ��ʾ:

�ش���������:
��1�� LiFePO4��Fe�Ļ��ϼ���_______________________��
��2����������������ǰ��Ҫ���з����������Ŀ����__________________________________��
��3�������ӷ���ʽ��ʾ����I�������۵�Ŀ��:__________________________������IIΪһϵ�в����������Ǽ���Ũ������ȴ�ᾧ�������������õ����մ�������������___________��
��4��TiO2+��ˮ��������ˮ������ӷ���ʽΪ______________________����ת�������õ���TiO2+��ˮ���������Ҫ����Һ���ȣ����ȵ�Ŀ����________________________________��
��5�����������ĵ���ʹFe3+����FePO4������Һ��c(PO43-)= 1.0��10-17mol/Lʱ����ΪFe3+ ������ȫ������Һ��Fe3+������ȫʱ��c(Fe3+)=_______mol/L[��֪:���¶�����Ksp(FePO4)=1.0��10-22]��
��6���������������Ʊ�LiFePO4�Ĺ����У�����17% H2O2��Һ�����( H2C2O4)����������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M ��ij���ϵ���Ч�ɷ֣�������к� 3 ����Ԫ����M ��һ�ֺϳ�·�����£�
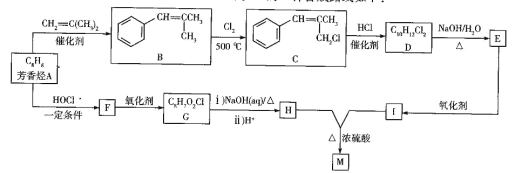
��֪����A ����������ԭ�ӿ��ܹ�ƽ�棻��D �ĺ˴Ź�����������6���壻��H �� I ��Ϊͬϵ� ��ش��������⣺
(1)A ��������____________��E ������������������___________��
(2)B��C �ķ�Ӧ������____________��
(3)д�� H �� I ��Ӧ���� M �Ļ�ѧ����ʽ��___________��
(4)T�� H ��ͬ���칹�壬ͬʱ�߱�����������T��___________��(�����������칹)�����У�������һ�����ֻ�� 2 �ֵĽṹ��ʽΪ____________��
����FeCl3��Һ������ɫ��Ӧ�����ܷ���ˮ�ⷴӦ��������Ӧ��
(5)A ��( )��ҽҩ����㷺����������������������ܼ��ȡ������������̣��� 2����ϩ����ϩΪԭ�Ϻϳ����ᣬ��ƺϳ�·�ߣ�_____________________(���Լ���ѡ)��
)��ҽҩ����㷺����������������������ܼ��ȡ������������̣��� 2����ϩ����ϩΪԭ�Ϻϳ����ᣬ��ƺϳ�·�ߣ�_____________________(���Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2��һ�������ºϳɼ״��ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g) ��H1�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ�����ʵ�飬������������ͼ��ͼ1���¶ȷֱ�Ϊ300�� ��500����ܱ������У��״������ʵ�����ͼ2���¶ȷֱ�ΪTl��T5���ܱ������У���Ӧ�����е�5minʱ�״������������������������ȷ����
CH3OH(g) ��H1�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ�����ʵ�飬������������ͼ��ͼ1���¶ȷֱ�Ϊ300�� ��500����ܱ������У��״������ʵ�����ͼ2���¶ȷֱ�ΪTl��T5���ܱ������У���Ӧ�����е�5minʱ�״������������������������ȷ����
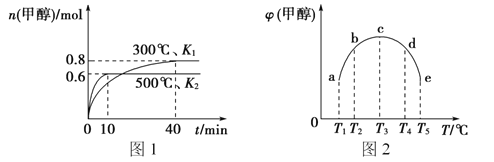
A. �÷�Ӧ�ġ�H1>0����K1>K2
B. ������c�е�ƽ��״̬ת�䵽����d�е�ƽ��״̬,�ɲ�ȡ�Ĵ�ʩ�����»��ѹ
C. 300��ʱ����ƽ�����������ٳ���0.8molCO, 0.6molH2��0.2molCH3OH��ƽ�������ƶ�
D. 500��ʱ����ƽ�����������ٳ���1molCH3OH������ƽ���H2Ũ�ȺͰٷֺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵����ȷ���ǣ� ��

A.ԭ�Ӱ뾶��W>Z
B.�����£�X�ĵ�����Y�ĵ��ʾ�������Ũ����
C.X������������ˮ������ǿ��
D.�����̬�⻯�����ȶ��ԣ�Z<W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ������������M��N���϶�����ͬ����Ԫ���һ�ѧ�������Ƶ��ǣ� ��
A.ԭ�Ӻ�������Ų�ʽ��MΪ1s22s2��NΪ1s2
B.�ṹʾ��ͼ��M![]() ��N
��N![]()
C.Mԭ�ӻ�̬2p�������һ�ԳɶԵ��ӣ�Nԭ�ӻ�̬3p�������һ�ԳɶԵ���
D.Mԭ�ӻ�̬2p�������1��δ�ɶԵ��ӣ�Nԭ�ӻ�̬3p�������1��δ�ɶԵ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com