
·ÖĪö £Ø1£©aŅĒĘ÷Ćū³ĘŹĒĒņŠĪĄäÄż¹Ü£Ø»ņĄäÄż¹Ü»ņĄäÄżĘ÷£©£»²śĪļÖŠŗ¬ÓŠĖ®£¬ĀČ»ÆĀĮŹōÓŚĒæĖįČõ¼īŃĪ£¬Ņ×Ė®½ā£»
ĀČ»ÆĀĮĖ®½āÉś³ÉHCl£¬HClÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬²»ÄÜÖ±½ÓÅÅæÕ£¬ĒŅ¼«Ņ×ČÜÓŚĖ®£»
£Ø2£©ĀČ»ÆĀĮŅ×Ė®½āÉś³ÉĒāŃõ»ÆĀĮ£¬øÉŌļ¹ÜÖŠĪļÖŹĪüŹÕĖ®ÕōĘų·ĄÖ¹ĀČ»ÆĀĮĖ®½ā£»
£Ø3£©µŚ¶ž“ĪĖ®Ļ“ÄæµÄŹĒĻ“Č„æÉČÜŠŌĪŽ»śĪļ£»ĪŽĖ®ĮņĖįĆ¾¾ßÓŠĪüĖ®ŠŌ£»
£Ø4£©ÕōĮóŹ±ĪĀ¶Č¼Ę²āĮæĮó·ÖĪĀ¶Č£»ĪĀ¶Č¼ĘĪ»ÖĆŌ½øߣ¬µĆµ½Įó·ÖĪĀ¶ČŌ½øߣ»
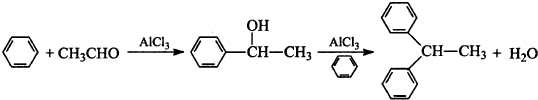
£Ø5£©øł¾ŻŌĮĻŗĶ×Ŗ»Æ¹ŲĻµæÉĻČ¼ĘĖć³ö1£¬1-¶ž±½ŅŅĶéµÄĄķĀŪ²śĮ棬ŌŁøł¾Ż²śĀŹ=$\frac{Źµ¼Ź²śĮæ}{ĄķĀŪ²śĮæ}$”Į100%¼ĘĖć1£¬1-¶ž±½ŅŅĶé²śĀŹ£»
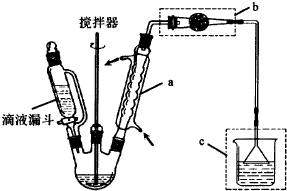
½ā“š ½ā£ŗ£Ø1£©aŅĒĘ÷Ćū³ĘŹĒĒņŠĪĄäÄż¹Ü£Ø»ņĄäÄż¹Ü»ņĄäÄżĘ÷£©£»ĀČ»ÆĀĮŹōÓŚĒæĖįČõ¼īŃĪ£¬Ņ×Ė®½ā£¬²śĪļÖŠŗ¬ÓŠĖ®£¬ĖłŅŌĀČ»ÆĀĮĖ®½āÉś³ÉĒāŃõ»ÆĀĮŗĶHCl£¬Ė®½ā·½³ĢŹ½ĪŖAlCl3+3H2O?Al£ØOH£©3+3HCl£»
ĀČ»ÆĀĮĖ®½āÉś³ÉHCl£¬HClÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬²»ÄÜÖ±½ÓÅÅæÕ£¬ĒŅ¼«Ņ×ČÜÓŚĖ®£¬ĖłŅŌÓĆĖ®ĪüŹÕÉś³ÉµÄHCl£¬ĪŖ·ĄÖ¹µ¹Īü£¬Ī²Ęų“¦Ąķ×°ÖĆĮ¬½Óµ¹ÖĆĀ©¶·£¬
¹Ź“š°øĪŖ£ŗĒņŠĪĄäÄż¹Ü£Ø»ņĄäÄż¹Ü»ņĄäÄżĘ÷£©£»AlCl3+3H2O?Al£ØOH£©3+3HCl£»ĪüŹÕHClĘųĢ壻
£Ø2£©Ī²Ęų“¦Ąķ×°ÖĆÖŠÓĆĖ®×÷ĪüŹÕ¼Į£¬ĀČ»ÆĀĮŅ×Ė®½āÉś³ÉĒāŃõ»ÆĀĮ£¬ĪŖ·ĄÖ¹ÉÕ±ÖŠµÄĖ®ÕōĘų½ųČė·“ӦװÖĆÖŠ£¬ĖłŅŌÓĆøÉŌļ¹ÜÖŠĪļÖŹĪüŹÕĖ®ÕōĘų£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹ÉÕ±ÖŠµÄĖ®ÕōĘų½ųČė·“Ó¦Ę÷ÖŠÓėČżĀČ»ÆĀĮ·“Ó¦£»
£Ø3£©µŚ¶ž“ĪĖ®Ļ“ÄæµÄŹĒĻ“Č„æÉČÜŠŌĪŽ»śĪļ£¬ČēĀČ»ÆĀĮ”¢ŃĪĖįŗĶĢ¼ĖįÄĘ£»
ĪŽĖ®ĮņĖįĆ¾¾ßÓŠĪüĖ®ŠŌ£¬ÄÜ×÷øÉŌļ¼Į£¬ĖłŅŌĪŽĖ®ĮņĖįĆ¾µÄ×÷ÓĆŹĒ×÷øÉŌļ¼Į£¬
¹Ź“š°øĪŖ£ŗĻ“µōĀČ»ÆĀĮ”¢ŃĪĖįŗĶĢ¼ĖįÄĘ£Ø»ņĻ“µōæÉČÜŠŌĪŽ»śĪļ£©£»øÉŌļ£»
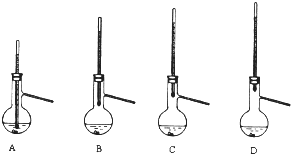
£Ø4£©ÕōĮóŹ±ĪĀ¶Č¼Ę²āĮæĮó·ÖĪĀ¶Č£¬ĖłŅŌĪĀ¶Č¼ĘĖ®ŅųĒņĪ»ÓŚÉÕĘæÖ§¹ÜæŚ“¦£»ĪĀ¶Č¼ĘĪ»ÖĆŌ½øߣ¬µĆµ½Įó·ÖĪĀ¶ČŌ½øߣ¬æÉÄÜ»įµ¼ÖĀŹÕ¼Æµ½µÄ²śĘ·ÖŠ»ģÓŠµĶ·ŠµćŌÓÖŹµÄ×°ÖĆŹĒAB£¬¹Ź“š°øĪŖ£ŗC£»AB£®
£Ø5£©øł¾ŻĢāÖŠĢõ¼žæÉÖŖ£¬±½µÄĪļÖŹµÄĮæĪŖ$\frac{140”Į0.88}{78}$mol=1.58mol£¬ŅŅČ©µÄĪļÖŹµÄĮæĪŖ$\frac{5.5}{44}$mol=0.125mol£¬øł¾ŻĪļÖŹ×Ŗ»Æ¹ŲĻµ£¬±½¹żĮ棬ĖłŅŌ1£¬1-¶ž±½ŅŅĶéµÄĄķĀŪ²śĮæĪŖ0.125”Į£Ø77+77+28£©g=22.75£¬ĖłŅŌ1£¬1-¶ž±½ŅŅĶéµÄ²śĀŹ=$\frac{Źµ¼Ź²śĮæ}{ĄķĀŪ²śĮæ}$”Į100%=$\frac{12.5g}{22.75g}$”Į100%=55%£¬
¹ŹŃ”C£»
µćĘĄ ±¾Ģāæ¼²éÖʱøŹµŃé·½°øÉč¼Ę£¬²ąÖŲæ¼²éѧɜ·ÖĪö”¢»ł±¾²Ł×÷µČÄÜĮ¦£¬Ć÷Č·ŹµŃéŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬ÖŖµĄĆæøöŅĒĘ÷×÷ÓĆ”¢ĪļÖŹµÄŠŌÖŹ£¬Ń§Éś¶ŌÓŚÖʱøŹµŃé½ĻÄ°Éś£¬¶ŌÓŚÓŠ»śĪļŠŌÖŹ½ĻÄ°Éś£¬“Ó¶ųµ¼ÖĀµĆ·ÖĀŹ½ĻµĶ£¬ĪŖѧĻ°ÄŃµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆCuSO4ČÜŅŗ½«ZnS×Ŗ»Æ³ÉCuS³Įµķ£ŗS2-+Cu2+ØTCuS”ż | |
| B£® | NH4HCO3ČÜŅŗÓė¹żĮæNaOHČÜŅŗ»ģŗĻ¼ÓČČ£ŗNH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+H2O | |
| C£® | ĻņĖį»ÆµÄFeSO4ČÜŅŗÖŠµĪČėÉŁĮæH2O2ČÜŅŗ£ŗH2O2+2Fe2++2H+ØT2Fe3++2H2O | |
| D£® | ÓƶčŠŌµē¼«µē½ā±„ŗĶµÄKClČÜŅŗ£ŗ2H++2Cl$\frac{\underline{\;Ķصē\;}}{\;}$H2”ü+Cl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŌŖĖŲ“śŗÅ | X | Y | Z | W |
| Ō×Ó°ė¾¶/pm | 160 | 143 | 70 | 66 |
| Ö÷ŅŖ»ÆŗĻ¼Ū | +2 | +3 | +5”¢+3”¢-3 | -2 |
| A£® | X”¢YŌŖĖŲµÄ½šŹōŠŌX£¼Y | |
| B£® | Ņ»¶ØĢõ¼žĻĀ£¬Zµ„ÖŹÓėWµÄ³£¼ūµ„ÖŹÖ±½ÓÉś³ÉZW2 | |
| C£® | YµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜČÜÓŚĻ”°±Ė® | |
| D£® | Ņ»¶ØĢõ¼žĻĀ£¬Wµ„ÖŹæÉŅŌŗĶZµ„ÖŹŌŚ·ÅµēĢõ¼žĻĀ·¢Éś»ÆŗĻ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĽųĘū³µĪ²Ęų¾»»Æ¼¼Źõ£¬¼õÉŁ“óĘųĪŪČ¾ĪļµÄÅÅ·Å | |
| B£® | æŖ·¢ĄūÓĆæÉŌŁÉśÄÜŌ“£¬¼õÉŁ»ÆŹÆČ¼ĮĻµÄŹ¹ÓĆ | |
| C£® | ¹ż¶ČæŖ²ÉæóĪļ׏Ō“£¬“Ł½ųµŲ·½¾¼Ć·¢Õ¹ | |
| D£® | ŃŠ·¢æɽµ½āøß·Ö×Ó²ÄĮĻ£¬¼õÉŁ”°°×É«ĪŪČ¾”± |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na | B£® | Si | C£® | P | D£® | S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬»ÆŗĻĪļABFµÄµē×ÓŹ½ĪŖ
£¬»ÆŗĻĪļABFµÄµē×ÓŹ½ĪŖ £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ¶¼ŹĒ³£ÓƵ÷Ī¶Ę·µÄÖ÷ŅŖ³É·Ö | B£® | ¶¼ÄÜŹ¹×ĻÉ«ŹÆČļČÜŅŗĶŹÉ« | ||
| C£® | ¶¼ÄÜŗĶCaCO3·“Ó¦ | D£® | ¶¼ÄÜ·¢Éśõ„»Æ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com