
����Ŀ���������Һ�絼��Խ������Խǿ����������0.100mol��L-1����ֱ�ζ�10.00mLŨ�Ⱦ�Ϊ0.100mol��L��1��NaOH��Һ�Ͷ��װ�[(CH3)2NH]��Һ(���װ���ˮ�е����백���ƣ�����Kb[(CH3)2NH��H2O]��1.6��10��4�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵����ȷ���ǣ� ��
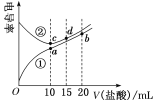
A.���ߢڴ����ζ����װ���Һ������
B.a����Һ�У�c(H��)��c(OH��)��c[(CH3)2NH��H2O]
C.d����Һ�У�2c(Na��)��3c(Cl��)
D.����ͬ�¶��£�a��b��c��d�ĵ����Һ�У�ˮ�ĵ���̶�������c��
���𰸡�B
��������
�������Һ�絼��Խ������Խǿ���������Һ�ĵ�������������Ũ���Լ�����������йأ�NaOHΪǿ����װ�Ϊ�����˿�ʼʱ�絼��������NaOH���絼��С���Ƕ��װ��������ߢ�Ϊ����ζ����װ������ߣ����ߢ�Ϊ����ζ�NaOH�����ߣ��ݴ˷�����
A���������Һ�絼��Խ������Խǿ���������Һ�ĵ�������������Ũ���Լ�����������йأ�NaOHΪǿ����װ�Ϊ�����˿�ʼʱ�絼��������NaOH���絼��С���Ƕ��װ��������ߢ�Ϊ����ζ����װ������ߣ����ߢ�Ϊ����ζ�NaOH�����ߣ���A����
B��a���������Ϊ10mL������ǡ����ȫ��Ӧ������Ϊ(CH3)2NH2Cl�����������غ㣬�ó���c(H��)=c(OH��)��c[(CH3)2NH��H2O]����B��ȷ��
C��d����Һ��n(Cl��)=15��10��3L��0.100mol��L��1��n(Na��)=10.00L��10��3L��0.100mol��L��1������3c(Na��)=2c(Cl��)����C����
D����������������a������Ϊ(CH3)2NH2Cl��Ϊǿ�������Σ��ٽ�ˮ�ĵ��룬c������ΪNaCl����ˮ�ĵ�����Ӱ�죬b������Ϊ(CH3)2NH2Cl��HCl������ˮ�ĵ��룬d������ΪNaCl��HCl������ˮ�ĵ��룬ˮ�ĵ���̶�������a�㣬��D����
��ΪB��


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������;�㷺��ij��������Ҫ�ɷ���NiFe2O4(������)��NiO��FeO��CaO��SiO2�ȣ�����ͼ�ǴӸÿ����л���NiSO4�Ĺ���·�ߣ�
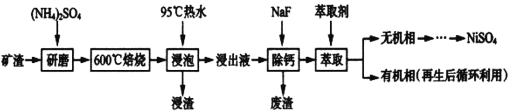
��֪��(NH4)2SO4��350�����ϻ�ֽ�����NH3��H2SO4��NiFe2O4�ڱ��չ���������NiSO4��Fe2(SO4)3����(Sn)λ�ڵ������ڵ�IVA�塣
��1������ǰ��������(NH4)2SO4�����ĥ�������ĥ��Ŀ����_______________��
��2�������ݡ�������Fe2(SO4)3����FeO(OH)�����ӷ���ʽΪ_________________________�����������ijɷֳ�Fe2O3��FeO(OH)�����___________________(�ѧʽ)��
��3��Ϊ��֤��Ʒ���ȣ�Ҫ��⡰����Һ������������ȡһ������Ľ���Һ���������ữ����SnCl2����Fe3+��ԭΪFe2+������SnC12�����ʵ���������Fe3+���ʵ�����_____������ȥ������SnCl2����������K2Cr2O7����Һ�ζ���Һ�е�Fe2+����ԭ����ΪCr3+���ζ�ʱ��Ӧ�����ӷ���ʽΪ_________________________________________��
��4��������Һ����c(Ca2+)=1.0��10-3mol��L-1���������ʴﵽ99��ʱ����Һ��c(F-)=___mol�� L-1��[��֪KSP(CaF2)=4.0��10-11]
��5����֪��ʮ����������ù��յ���ȡ�����õ绯ѧ�Ʊ���ʮ����ķ���Ϊ�����ձ��м���50mL�״������Ͻ���������������ƣ��ټ���11mL�����������ȣ�װ�ò��缫����ͨ��Դ��Ӧ�����������Լ�Сʱ�жϵ�Դ��Ȼ���ᴿ��ʮ���顣��֪����ܷ�ӦΪ��2C6H13COONa+2CH3OH![]() C12H26+2CO2��+H2��+2CH3ONa���������ĵ缫��ӦʽΪ______________________________________
C12H26+2CO2��+H2��+2CH3ONa���������ĵ缫��ӦʽΪ______________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����28.8gͭ��150mLһ��Ũ�ȵ����ᷴӦ��ͭ��ȫ�ܽ⣬������NO��NO2��������ڱ�״���µ����Ϊ11.2L����ش�
��1��NO�����Ϊ___L��NO2�����Ϊ___L��
��2��������������ȫ���ͷţ�����Һ�м���200mL5mol��L-1��NaOH��Һ��ǡ��ʹ��Һ�е�Cu2+ȫ��ת���ɳ�������ԭ������Һ��Ũ��Ϊ___mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����պ�����CO2�ǻ�����ѧ���о����ȵ㣬�Ǽ�������ЧӦΣ������Ҫ;����
(1)��̫���ܵ������£���CO2Ϊԭ����ȡ̿�ڵ�������ͼ��ʾ�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_____________��
(2)CO2�������⻯�ϳɵ�̼ϩ�����ϳ���ϩ�ķ�ӦΪ
2CO2(g)+6H2(g)==CH2=CH2(g)+4H2O(g) ��H=akJ/mol
��֪:
�� | H-H | C=O | C=C | O-H | C-H |
����/kJ/mol | 436.0 | 745.0 | 615.0 | 462.8 | 413.4 |
��a=________��
(3)T��ʱ���ں����ܱ������г���1molCO2��nmolH2����һ�������·�����Ӧ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H<0�����������CH3OH ��������������������ʵ����Ĺ�ϵ��ͼ��ʾ��ͼ1��A��B��C �����Ӧ����ϵ��CO��ת����������____(����ĸ)���ж�������____________��
CH3OH(g)+H2O(g) ��H<0�����������CH3OH ��������������������ʵ����Ĺ�ϵ��ͼ��ʾ��ͼ1��A��B��C �����Ӧ����ϵ��CO��ת����������____(����ĸ)���ж�������____________��


(4) ��ҵ��Ҳ�úϳ���(H2��CO) �ϳɼ״�����ӦΪ2H2(g)+CO(g)![]() CH3OH(g) ��H<0����10L�ĺ������������г���H2��CO�����ʵ����ֱ�Ϊ2mol��1mol�����CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ2��ʾ��
CH3OH(g) ��H<0����10L�ĺ������������г���H2��CO�����ʵ����ֱ�Ϊ2mol��1mol�����CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ2��ʾ��
��ͼ2��S��������������_________��
����֪300��ʱ������Ӧ�ﵽƽ��ʱ��CO ��ƽ��ת����Ϊ60% �������ƽ����ϵ���ټ���2molCO��2molH2��2molCH3OH �������¶Ⱥ������ݻ����䣬��ƽ���_____(������ƶ����������ƶ������ƶ���)��
(5)��ҵ�ϳ��ø�Ũ�ȵ�K2CO3��Һ����CO2������ҺX�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ����ͼ��ʾ��

������������CO2��ԭ����________(�����ӷ���ʽ��ʾ)��
������ƽ���ƶ�ԭ��������CO32-��������������ԭ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
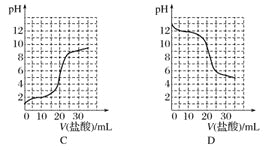
����Ŀ����֪ij�¶���CH3COOH�ĵ��볣��K��1.6��10-5 mol��L-1�����¶��£���20mL0.01 mol��L-1CH3COOH��Һ����μ���0.01mol��L-1KOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯����
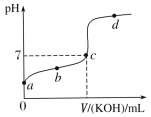
��ش������й����⣺
��1��a��b��c��d�ĵ���ˮ�ĵ���̶�������___�㡣
��2������20mLϡ��ˮ����μ����Ũ�ȵ����ᣬ�����б仯������ȷ����___����ţ���
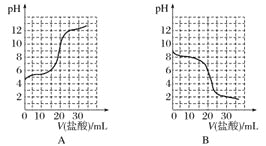
��3����FeCl3��Һ�������ɣ����գ��ù�������Ϊ___���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����4��̼ԭ�ӽ�ϳɵ�6���л���(��ԭ��û�л���)
![]()
(1) д���л���(a)��ϵͳ������������___________________��
(2) �л���(a)��һ��ͬ���칹�壬��д����ṹ��ʽ__________________��
(3) �����л�������(c)��Ϊͬ���칹�����________(�����)��
(4) ��дһ����(e)��Ϊͬϵ����л���Ľṹ��ʽ____________��
(5) �����л����в������巴Ӧ��ʹ����ɫ����________(�����)��
(6) (a)(b)(c)(d)���������У�4��̼ԭ��һ������ͬһƽ�����________(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ1 L���ܱ������У�1 mol X��1 mol Y���з�Ӧ��2X(g) ��Y(g)![]() Z(g)������������֤���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
Z(g)������������֤���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
A.X�İٷֺ������ٷ����仯
B.c(X)��c(Y)��c(Z)��2��1��1
C.������ԭ���������ٷ����仯
D.ͬһʱ��������2n mol X��ͬʱ����n mol Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2CO3��Һ�еμ����ᣬ��Ӧ�����������仯����ͼ��ʾ������˵����ȷ���ǣ� ��
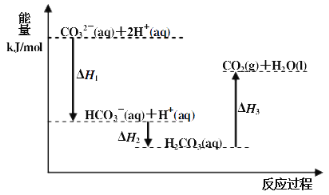
A.��ӦHCO3-(aq)+H+(aq)��CO2(g)+H2O(l) Ϊ���ȷ�Ӧ
B.CO32-(aq)+2H+(aq)��CO2(g)+H2O(l) H��(H1+H2+H3)
C.H1��H2 H2��H3
D.H2CO3(aq)��CO2(g)+H2O(l)����ʹ�ô�������H3��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ�ĵ���( )
ѡ�� | ���� | Ŀ�� |
A | �÷�̪��ָʾ�����ñ���c mol��L��1����ζ�һ�����δ֪Ũ�ȵ� | �ⶨ |
B | ��һ���� | ����һ�����ʵ���Ũ�ȵ� |
C | �������Ƭ��ʯ���ͼ�ǿ�ȣ���������ͨ�����Ը��������Һ�� | ֤��������ﺬ̼̼˫�� |
D | �� | ֤�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com