
| A.凡是放热反应都是自发的 |
| B.难溶电解质的溶解平衡是一种动态平衡 |
| C.利用沉淀反应除杂时,可使杂质离子完全沉淀 |
| D.pH=5的盐酸稀释1000倍后,溶液的pH增到8 |
科目:高中化学 来源:不详 题型:单选题
| A.向醋酸钠溶液中加水稀释时,溶液中所有离子浓度都减小 |
| B.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<0,则该反应一定能自发进行 |
D.对N2(g)+3H2(g) 2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
 0(填“>’或“<”)。
0(填“>’或“<”)。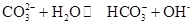 ,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
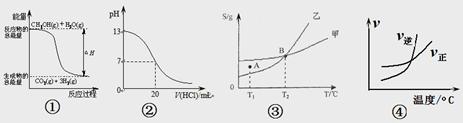
| A.根据图①可判断反应CH3OH(g)+H2O(g)=CO2(g)+3H2(g)的ΔH<0 |
| B.图②表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液的pH随加入酸体积的变化 |
| C.根据图③(S表示溶解度),A点表示T1oC时甲为饱和溶液,乙溶液未饱和。 |
D.根据图④可判断可逆反应“A2(g)+3B2(g) 2AB3(g)”的ΔH>0 2AB3(g)”的ΔH>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2+I2
H2+I2
 2HI(g)的平衡常数K=__________________
2HI(g)的平衡常数K=__________________查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g) + H2(g)△H1=" +" 41.2kJ/mol
CO2(g) + H2(g)△H1=" +" 41.2kJ/mol CO2(g) + H2(g)△H1=" +" 41.2kJ/mol
CO2(g) + H2(g)△H1=" +" 41.2kJ/mol查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知常温常压下4Fe(s)+3O2(g)=2Fe2O3(s)是自发反应, 则该反应是吸热反应 |
| B.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
C.一定条件下2molPCl3和2molCl2发生反应PCl3(g)+Cl2(g)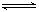 PCl5(g) ΔH= -93kJ?mol—1 ,达平衡时放热139.5kJ,则PCl3的转化率为75% PCl5(g) ΔH= -93kJ?mol—1 ,达平衡时放热139.5kJ,则PCl3的转化率为75% |
| D.用pH分别为2和3的醋酸中和等量的NaOH,消耗醋酸的体积分别为V1和V2,则V1>10V2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com