

| A. | 用pH试纸测定浓硫酸的pH | |
| B. | 向碘酒中加入CCl4,静置后分液,可以分离碘酒中的碘 | |
| C. | 用甲图装置验证FeCl3对H2O2分解反应有催化作用 | |
| D. | 用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
分析 A.浓硫酸具有脱水性和强腐蚀性,能使纸张脱水、被氧化;
B.乙醇和四氯化碳互溶;
C.要验证FeCl3对H2O2分解反应有催化作用,需要对比实验;
D.碳酸氢钠不稳定,受热易分解,碳酸钠较稳定,受热不易分解.
解答 解:A.浓硫酸具有脱水性和强腐蚀性,能使纸张脱水、被氧化,所以不能用pH试纸测定浓硫酸的pH值,应该用pH计,故A错误;
B.乙醇和四氯化碳互溶,所以不能用四氯化碳作碘酒的萃取剂,故B错误;
C.要验证FeCl3对H2O2分解反应有催化作用,需要对比实验,该实验没有对比装置,所以不能实现实验目的,故C错误;
D.碳酸氢钠不稳定,受热易分解,碳酸钠较稳定,受热不易分解,如果温度低时碳酸氢钠都分解生成二氧化碳,则说明碳酸钠比碳酸氢钠稳定,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及pH值的测定、萃取、探究化学反应速率影响因素、物质稳定性判断等知识点,明确实验原理、物质性质差异性、实验基本操作是解本题关键,注意C中应该有对比实验才能做出正确判断,否则无法判断,为易错点.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:实验题
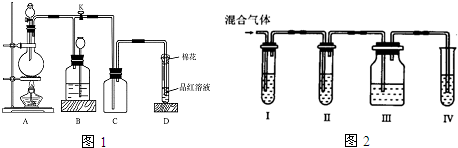
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
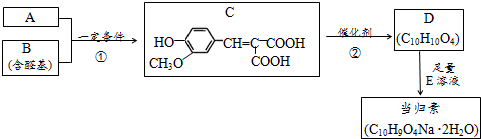
 ;
;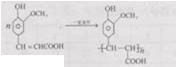 ;
;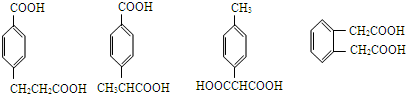 (其中两种).
(其中两种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯醛的结构简式:CH2═CHCHO | |
| B. | CSO的电子式: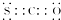 | |
| C. | 硫酸氢钠熔融时的电离方程式:NaHSO4═Na++HSO4- | |
| D. | S2-的结构示意图: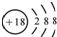 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
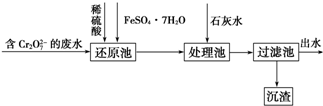
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
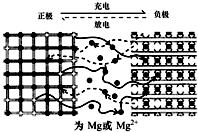 镁离子电池以金属镁或镁合金为负极,以能嵌入镁离子的化合物为正极,其工作原理如图所示,反应原理为:xMg+Mo3S4$?_{充电}^{放电}$ MgxMo3S4,下列说法不正确的是( )
镁离子电池以金属镁或镁合金为负极,以能嵌入镁离子的化合物为正极,其工作原理如图所示,反应原理为:xMg+Mo3S4$?_{充电}^{放电}$ MgxMo3S4,下列说法不正确的是( )| A. | 放电时,电池中的Mg2+从负极移向正极 | |
| B. | 其负极反应为:xMg-2xe-+Mo3S42x-═MgxMo3S4 | |
| C. | 充电时阳极反应式:MgxMo3S4-2xe-═Mo3S4+xMg2+ | |
| D. | 由于镁的密度较小,且Mg2+携带两个正电荷,这为高能量电池的设计提供了一个可靠依据 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12m) | 37 | 71 | 74 | 77 | 186 |
| 主要化合价 | +1 | -1 | -2 | +4、-4 | +1 |
| A. | X和Q都属于金属元素 | |
| B. | Y和Z的基态原子s能级和p能级电子数相同 | |
| C. | Y和W的第一电离能大小比较:Y>W | |
| D. | X、Z形成的化合物分子中可能既有σ键又有π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素化合价升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com