
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源:2015-2016学年湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类。下列叙述错误的是( )
A.等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等
B.废弃的PE和PVC均可回收利用以减少白色污染
C.将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红
D.PVC的单体可由PE的单体与氯化氢加成制得
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练五化学试卷(解析版) 题型:选择题
某芳香族化合物甲的分子式为C10H11ClO2,已知苯环上只有两个取代基,其中一个取代基为-Cl,甲能与饱和碳酸氢钠溶液反应放出二氧化碳,则满足上述条件的有机物甲的同分异构体数目有多少种( )
A.5种 B.9种 C.12种 D.15种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二下第十二周练化学卷(解析版) 题型:选择题
下列溶液中不存在配离子的是
A.CuSO4水溶液 B.银氨溶液 C.硫氰化铁溶液 D.I2的CCl4溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:填空题
已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素。
(1)写出C元素的原子结构示意图____________________,用电子式写出C和E形成化合物的过程___________________,用电子式写出A和B形成化合物的过程_____ _______。
(2)B元素的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在化学键的类型为
(3)C元素的最高价氧化物对应的水化物与D元素的最高价氧化物反应的离子方程式为 。
(4)已知X、Y、Z三种物质中均含有上述元素中的某一种元素,它们之间存在如图所示转化关系。

①X、Y、Z均含有上述元素中的同一种金属元素,若W固体俗称干冰,则反应Y→Z的离子方程为 ;
②X、Y、Z均含有上述元素中的同一种金属元素,若W是强碱,且Y为白色难溶固体,则反应Z→Y的离子方程式为________________________。
③X、Y、Z是均含有上述元素中的同一种非金属元素的化合物,W是一种常见金属单质,且上述转化均在常温条件下完成,则反应Z→Y的离子方程式__________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
元素R有如下反应:RO3-+5R-+6H+=3R2+3H2O,下列说法正确的是
A.元素R位于周期表中第ⅤA族 B.RO3-中的R只能被还原
C.R2在常温常压下一定是气体 D.反应每消耗1 mol RO3-,转移电子的物质的量为5 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
下列反应属于吸热反应的是
A.稀硫酸与氢氧化钠溶液反应 B.碳和二氧化碳生成一氧化碳的反应
C.锌与稀硫酸的反应 D.生石灰变成熟石灰的反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:选择题
下列实验操作与实验目的都正确的是
实验操作 | 实验目的 | |
A | 制乙炔时用饱和食盐水代替水 | 加快化学反应速率 |
B | CH4与SO2混合气体通过盛有溴水的洗气瓶 | 除去中CH4的SO2 |
C | 甲烷与乙烯的混合气体通过盛有酸性高锰酸钾的洗气瓶 | 除去甲烷中的乙烯 |
D | 将浓硫酸、乙醇混合加入试管中,加热,然后将导管末端插入酸性KMnO4溶液中,观察现象; | 检验是否有乙烯生成 |
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:填空题
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用.
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体.已知室温下,1g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式______________。
(2)298K时,在2L的密闭容器中,发生可逆反应2NO2(g) N2O4(g)△H=-a kJ•mol-1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
N2O4(g)△H=-a kJ•mol-1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
①298k时,该反应的平衡常数为______________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是______________
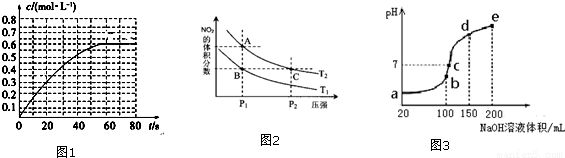
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6mol n(N2O4)=1.2mol,则此时V(正)______________V(逆)(填“>”、“<”或“=”).
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示。试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是______________;
②其溶液中c(OH-)的数值最接近NH3•H2O的电离常数K数值的是______________;
③在c点,溶液中各离子浓度由大到小的排列顺序是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com