
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-甲基-3-乙基戊烷 | D. | 2,2,3-三甲基丁烷 |
分析 A、丁烷最长碳链为4,在2、3号碳上能含有甲基;
B、丁烷最长碳链为4,命名选取代数和最小;
C、戊烷最长碳链为5,在2、3号碳上分别含有甲基和乙基;
D、丁烷最长碳链为4,在2、3号碳上分别含有甲基1个和2个甲基.
解答 解:A、2,3-二甲基丁烷,符合系统命名法,故A正确;
B、3,3-二甲基丁烷,选取的支链代数和不是最小,不符合系统命名法,正确应为2,2-二甲基丁烷,故B错误;
C、2-甲基-3-乙基戊烷,符合系统命名法,故C正确;
D、2,2,3-三甲基丁烷,符合系统命名法,故D正确;
故选B.
点评 本题主要考查了有机物的命名知识.一般要求了解烷烃的命名,命名时要遵循命名原则,书写要规范.


科目:高中化学 来源: 题型:选择题
| A. | 核外电子质量很小,在原子核外作高速运动 | |
| B. | 核外电子的运动规律与普通物体不同 | |
| C. | 在电子云示意图中,通常用小黑点来表示电子 | |
| D. | 在电子云示意图中,小黑点密表示电子在核外空间单位体积内电子出现的机会多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,请按要求完成下列问题:
,请按要求完成下列问题: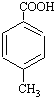 ;
;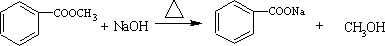 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素都是碱金属元素 | |
| B. | 碱金属单质可将铜从其盐溶液中置换出来 | |
| C. | 金属钾具有强还原性,K+具有强氧化性 | |
| D. | Cs常温下与水反应会发生爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 牛油、纤维素和蛋白质都是天然高分子化合物 | |
| B. | 淀粉可以使碘化钾试纸变蓝 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
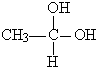 →CH3-CHO+H2O
→CH3-CHO+H2O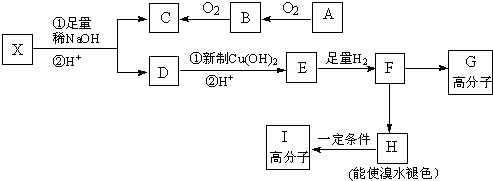
 ;
;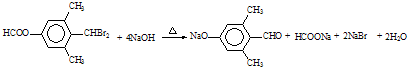 ;
;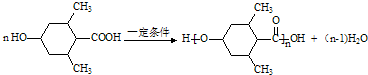 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
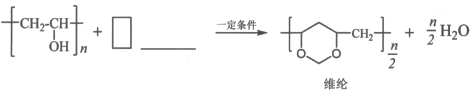
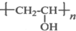 ,其工业合成路线如下:
,其工业合成路线如下: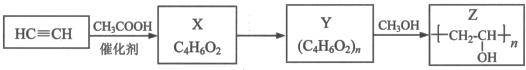
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
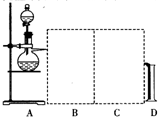
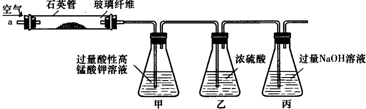
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com