
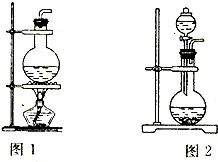
 依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.
依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套. NH3.H2O
NH3.H2O NH4++OH-,逆向移动,有利于氨气逸出;
NH4++OH-,逆向移动,有利于氨气逸出; NH3.H2O
NH3.H2O NH4++OH-,逆向移动,有利于氨气逸出.
NH4++OH-,逆向移动,有利于氨气逸出.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 为了研究外界条件对H2O2分解反应速率的影响,某同学在四支试管中分别加入3mLH2O2溶液,并测量收集VmL气体所需的时间,实验记录如下:
为了研究外界条件对H2O2分解反应速率的影响,某同学在四支试管中分别加入3mLH2O2溶液,并测量收集VmL气体所需的时间,实验记录如下:| 实验序号 | H2O2溶液浓度 | H2O2溶液温度 | 催化剂 | 所用时间 |
| ① | 5% | 20℃ | 2滴1mol/LFeCl3 | t1 |
| ② | 5% | 40℃ | 2滴1mol/LFeCl3 | t2 |
| ③ | 10% | 20℃ | 2滴1mol/LFeCl3 | t3 |
| ④ | 5% | 20℃ | 不使用 | t4 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
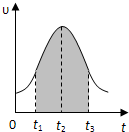 I.实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.回答如下问题:
I.实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.回答如下问题:
| V | 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.
依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com