
| A、Cu(OH)2>CuCO3>CuS |
| B、CuS>Cu(OH)2>CuCO3 |
| C、CuS<Cu(OH)2<CuCO3 |
| D、Cu(OH)2<CuCO3<CuS |


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
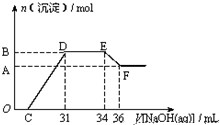 某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )
某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )| A、NH4NO3 |
| B、NO2 |
| C、NO |
| D、N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(H2O) |
| n(CH4) |
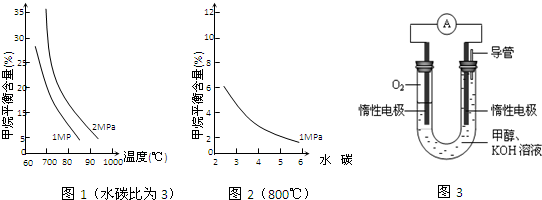
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 环境污染 |  白色污染 |
 雾霾 |
 臭氧空洞 |
 酸雨 |
| 产生原因 | 生活污水的排放 | 汽车尾气的排放 | 氟利昂的使用 | 煤的直接燃烧 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH
| ||
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | ||
C、室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中
| ||
| D、在0.1 mol?L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、实验Ⅰ:配置一定物质的量浓度的溶液 |
| B、实验Ⅱ:除去Cl2中的HCl |
| C、实验Ⅲ:用水吸收NH3 |
| D、实验Ⅳ:石油的分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 与 与 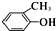 属于同素异形体 属于同素异形体 |
| B、CH3COOH与硬脂酸(C17H35COOH)属于同系物 |
C、 与 与  属于同一种物质 属于同一种物质 |
D、 与 与 属于同分异构体 属于同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com