
【题目】金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3++Fe3+。下列说法正确的是( )
A. Ce元素位于元素周期表第六周期第IIIB族
B. ![]() 、
、![]() 是同素异形体
是同素异形体
C. 铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
D. 铈的原子核外有58个电子
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 棉花和蚕丝的主要成分都是纤维素
B. 蛋白质在一定条件发生水解反应生成葡萄糖
C. 煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程
D. 食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
序号 | ||||
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是_________(填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。

①门捷列夫将已有元素按照相对原子质量排序,同一_________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_________,第5列方框中“Te=128?” 的问号表达的含义是_________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_________(填字母序号)。
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5。其余信息如图所示:
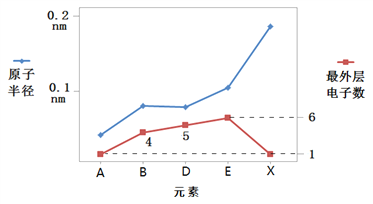
①上述七种元素中,处于第二周期的有_________(用元素符号表示,下同),X在周期表中的位置是_________。
②E的原子结构示意图为_________,写出Z元素气态氢化物的电子式:_________。
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为_________;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为_________。
④B和D的最高价氧化物的水化物的化学式分别为_________、_________,二者酸性前者_________(填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知实验室制备1,2﹣二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.现在用溴的CCl4溶液和足量的乙醇制备1,2﹣二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:
(1)制备1,2﹣二溴乙烷的合成路线
(2)在装置C中应加入 ,(填正确选项前的字母)其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)装置B的作用是 ;
(4)若产物中有少量副产物乙醚.可用 的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述不正确的是( )
A. 适当地摄入一定量的油脂,能促进脂溶性维生素的吸收
B. 蛋白质水解的最终产物是氨基酸
C. 葡萄糖在人体内发生氧化反应能放出大量热量
D. 淀粉、纤维素、油脂、蛋白质都是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠和钾的合金可用于快中子反应堆作热交换剂
B. 可用超纯硅制造的单晶硅来制芯片
C. 可利用二氧化碳制造全降解塑料
D. 氯气有毒,不能用于药物的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式为2Fe3++Fe=3Fe2+,以下不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为FeCl3
B.正极为C,负极为Fe,电解质溶液为Fe(NO3)3
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.SO2能使FeCl3,KMnO4水溶液褪色
B.可以用澄清石灰水鉴别SO2和CO2
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.少量SO2通过浓的CaCl2溶液能生成白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com