
| A. | NaOH | B. | Ba(NO3)2 | C. | Na2CO3 | D. | Ba(OH)2 |
分析 溶液导电性与离子浓度成正比,与电荷成正比,在硫酸溶液中加入溶液后,溶液导电性明显减小,说明混合溶液中离子浓度明显降低,据此分析解答.
解答 解:A.硫酸溶液中加入NaOH,二者反应生成硫酸钠和水,离子浓度变化不大,溶液导电性变化不大,故A不选;
B.二者反应生成硫酸钡和硝酸,离子浓度变化不大,溶液导电性变化不大,故B不选;
C.二者反应生成硫酸钠和水、二氧化碳,离子浓度变化不大,溶液导电性变化不大,故C不选;
D.二者反应生成硫酸钡沉淀和水,水电离程度很小,所以反应前后离子浓度变化很大,溶液导电性变化很大,故D选;
故选D.
点评 本题以溶液导电性强弱为载体考查离子反应,为高频考点,明确物质之间的反应及溶液导电性强弱影响因素是解本题关键,注意:溶液导电性强弱与离子浓度及离子所带电荷有关,与溶液酸碱性及物质溶解性强弱无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2KClO3(s)=2KCl(s)+3O2(g)△H=-78.03 kJ•mol-1,△S=494.4 J•mol-1•K-1 | |
| B. | CO(g)=C(s,石墨)+$\frac{1}{2}$O2(g)△H=110.5 kJ•mol-1,△S=-89.4 J•mol-1•K-1 | |
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)△H=-444.3 kJ•mol-1,△S=-280.1 J•mol-1•K-1 | |
| D. | NH4HCO3(s)+CH3COOH(aq)=CH3COONH4 (aq)+CO2(g)+H2O(l)△H=37.30 kJ•mol-1,△S=184.0 J•mol-1•K-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度,H2S浓度减小,表明该反应是放热反应 | |
| B. | 通入CO后,逆反应速率逐渐增大,直至再次平衡 | |
| C. | 反应前H2S物质的量为6mol | |
| D. | CO的平衡转化率为20% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
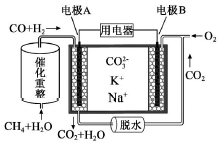
| A. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 反应CH4+H2O $\frac{\underline{催化剂}}{△}$ 3H2+CO,每消耗1molCH4转移12mol 电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量时,左盘高,右盘低 | |
| B. | 定溶时俯视容量瓶刻度线 | |
| C. | 原容量瓶洗净后未干燥 | |
| D. | 摇匀后见液面下降,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑦ | B. | ①③⑤⑥ | C. | ①③⑥⑦ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤⑦ | C. | ④⑧ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入银氨溶液,并水浴加热 | |
| B. | 加入2~3滴石蕊试液 | |
| C. | 先加入浓NaOH溶液,加热蒸馏,把蒸馏出的物质加银氨溶液并水浴加热 | |
| D. | 直接蒸馏,把蒸馏出的物质加NaOH溶液调至碱性,再加银氨溶液,并水浴加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com