
| A£® | ¼×ĶéµÄ±ź×¼Č¼ÉÕČČĪŖ-890.3 kJ•mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4£Øg£©+2O2£Øg£©ØTCO2£Øg£©+2H2O £Øg£©”÷H=-890.3 kJ•mol-1 | |
| B£® | ĻąĶ¬Ģõ¼žĻĀ£¬2molĒāŌ×ÓĖł¾ßÓŠµÄÄÜĮæŠ”ÓŚ1molĒā·Ö×ÓĖł¾ßÓŠµÄÄÜĮæ | |
| C£® | ³£ĪĀĻĀ£¬·“Ó¦C£Øs£©+CO2£Øg£©ØT2CO£Øg£© ²»ÄÜ×Ō·¢½ųŠŠ£¬ŌņøĆ·“Ó¦µÄ”÷H£¼0 | |
| D£® | ŅŃÖŖ¢Ł2H2£Øg£©+O2£Øg£©ØT2H2O £Øg£©”÷H1=a kJ•mol-1¢Ś2H2£Øg£©+O2£Øg£©ØT2H2O £Øl£©”÷H2=b kJ•mol-1£¬Ōņa£¾b |
·ÖĪö A£®Č¼ÉÕČČŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮæ·ÖĪö£»
B.2molĒāŌ×Ó±ä»ÆĪŖ1molĒā·Ö×ÓŹĒŠĪ³É»Æѧ¼üµÄ¹ż³Ģ£¬¹ż³ĢÖŠ·Å³öÄÜĮ棻
C£®·“Ó¦×Ō·¢½ųŠŠµÄÅŠ¶ĻŅĄ¾ŻŹĒ”÷H-T”÷S£¼0£»
D£®øĒĖ¹¶ØĀɼĘĖć¢Ł-¢ŚµĆµ½2H2O£Øl£©=2H2O£Øg£©”÷H=£Øa-b£©KJ/mol£¬ŅŗĢ¬Ė®±ä»ÆĪŖĘųĢ¬Ė®ĪüČČ£®
½ā“š ½ā£ŗA£®øł¾ŻČ¼ÉÕČȵÄøÅÄī£ŗ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļ£¬Ėł·Å³öµÄČČĮæĪŖČ¼ÉÕČČ£¬Ė®µÄדĢ¬Ó¦øĆĪŖŅŗĢ¬£¬¹ŹA“ķĪó£»
B.2molĒāŌ×Ó±ä»ÆĪŖ1molĒā·Ö×ÓŹĒŠĪ³É»Æѧ¼üµÄ¹ż³Ģ£¬¹ż³ĢÖŠ·Å³öÄÜĮ棬ĻąĶ¬Ģõ¼žĻĀ£¬2molĒāŌ×ÓĖł¾ßÓŠµÄÄÜĮæ“óÓŚ1molĒā·Ö×ÓĖł¾ßÓŠµÄÄÜĮ棬¹ŹB“ķĪó£»
C£®·“Ó¦×Ō·¢½ųŠŠµÄÅŠ¶ĻŅĄ¾ŻŹĒ”÷H-T”÷S£¼0£¬³£ĪĀĻĀ£¬·“Ó¦C£Øs£©+CO2£Øg£©ØT2CO£Øg£© ²»ÄÜ×Ō·¢½ųŠŠ”÷H-T”÷S£¾0£¬”÷S£¾0£¬ŌņøĆ·“Ó¦µÄ”÷H£¬£¾0£¬¹ŹC“ķĪó£»
D£®øĒĖ¹¶ØĀɼĘĖć¢Ł-¢ŚµĆµ½2H2O£Øl£©=2H2O£Øg£©”÷H=£Øa-b£©KJ/mol£¬ŅŗĢ¬Ė®±ä»ÆĪŖĘųĢ¬Ė®ĪüČČ£¬a-b£¾0£¬Ōņa£¾b£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éѧɜ·“Ó¦ČȵÄÓŠ¹ŲÖŖŹ¶£¬×¢Ņā¶ŌČ¼ÉÕČȵÄøÅÄīĄķ½āøĒĖ¹¶ØĀɵļĘĖćÓ¦ÓĆ£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al”¢Cu”¢AgNO3 | B£® | Na2O2”¢Na2SO3”¢BaCl2 | ||
| C£® | CaCO3”¢Na2SiO3”¢CH3COONa | D£® | Ba£ØNO3£©2”¢Fe£ØOH£©2”¢NaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
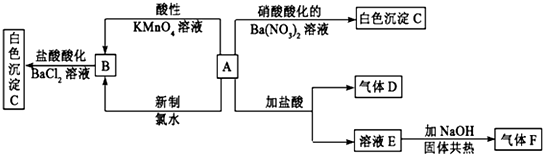
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al3+”¢NH4+”¢Cl-”¢SO42- | B£® | Na+”¢CH3COO-”¢K+”¢CO32- | ||
| C£® | Fe2+”¢Cl-”¢Na+”¢NO3- | D£® | K+”¢NO3-”¢Cl-”¢Na+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+£¼Mg2+£¼Al3+£¼K+ | B£® | S2-£¾Cl-£¾K+£¾Ca2+ | ||
| C£® | Cl£¾S£¾F£¾O | D£® | S2-£¾O2-£¾Cl-£¾Br- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CuO×÷»¹Ō¼Į | B£® | CuO×÷Ńõ»Æ¼Į | ||
| C£® | ĶŌŖĖŲ»ÆŗĻ¼Ū½µµĶ | D£® | ĒāŌŖĖŲ»ÆŗĻ¼ŪÉżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
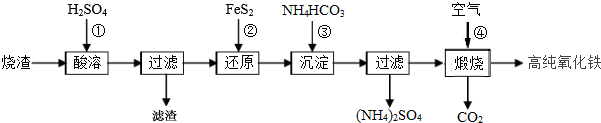
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com