
��12�֣��ȼ��ⱥ��ʳ��ˮ��ȡNaOH�Ĺ�������ʾ��ͼ���£�
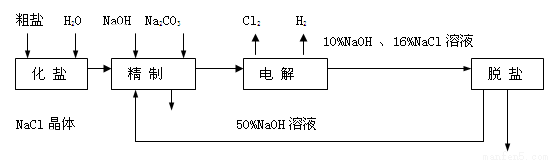
������ͼ�����������գ�
��1��д����ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ ��
��2�����������SO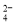 �����ϸߣ��������ӱ��Լ���ȥSO
�����ϸߣ��������ӱ��Լ���ȥSO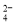 ���ñ��Լ������� ��ѡ��A��B��C����ѡ�۷֣�
���ñ��Լ������� ��ѡ��A��B��C����ѡ�۷֣�
A��Ba(OH)2 B��Ba(NO3)2 C��BaCl2
��3���жϱ��Լ��Ѿ������ķ����� ��
(4)Ϊ��Ч��ȥCa2+��Mg2+��SO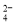 �������Լ��ĺ���˳��Ϊ ��ѡ��A��B��C��ѡ�۷֣�
�������Լ��ĺ���˳��Ϊ ��ѡ��A��B��C��ѡ�۷֣�
A���ȼ�NaOH��Һ�����Na2CO3��Һ���ټӱ��Լ�
B���ȼ�NaOH��Һ����ӱ��Լ����ټ�Na2CO3��Һ
C���ȼӱ��Լ������NaOH��Һ���ټ�Na2CO3��Һ
��5��Ϊ���龫�δ��ȣ�������150 mL0��2 mol/LNaCl�����Σ���Һ����ͼ�Ǹ�ͬѧת����Һ��ʾ��ͼ��
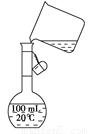
ͼ�еĴ����� ��
���ڸ����ƹ����У�����˵����ȷ����________��
A��Ӧ��ȡ�Ȼ��ƾ��������Ϊ1��755 g
B��ϴ��Һ����Ҫת�Ƶ�����ƿ��
C������ʱ������ͬѧ���ӣ�������������ҺŨ��ƫ��
D��ҡ�Ⱥ��ã�����Һ����ڿ̶��ߣ�Ӧ������ˮ����Һ����̶�������
��1��2NaCl+2H2O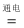 2NaOH+H2��+Cl2���� ��2�� C
2NaOH+H2��+Cl2���� ��2�� C
��3�����ã����ϲ���Һ�м����μ��Ȼ�����Һ���粻�������ѹ�����
(4)BC
��5������ƿ���ݻ�û��150ml û���ò��������� C
��������
�����������1����ⱥ��ʳ��ˮ�������������������������������������ƣ���Ӧ�Ļ�ѧ����ʽΪ2NaCl+2H2O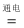 2NaOH+H2��+Cl2������2�����ݳ���ԭ�������������ʣ�����Ba(OH)2������OH- ������Ba(NO3)2������NO3-�����Կ�����BaCl2����3�����ã����ϲ���Һ�м����μ��Ȼ�����Һ���粻�������ѹ�����(4) Ϊ�˳�ȥ����Ĺ������Ȼ�����̼����һ��Ҫ�ڼ����Ȼ���֮����룬��BC��ȷ����5������150mL����Һ����Ҫ150mL������ƿ��������ƿ������ҺҪ�ò�����������������ƽ�ľ���Ϊ0��1g����A����ϴ��Һ��Ҫת�Ƶ�����ƿ�У���B��������ʹ��Һ���ƫ��Ũ��ƫС����C��ȷ��ҡ�Ⱥ��ã����ܼ�ˮ����D����
2NaOH+H2��+Cl2������2�����ݳ���ԭ�������������ʣ�����Ba(OH)2������OH- ������Ba(NO3)2������NO3-�����Կ�����BaCl2����3�����ã����ϲ���Һ�м����μ��Ȼ�����Һ���粻�������ѹ�����(4) Ϊ�˳�ȥ����Ĺ������Ȼ�����̼����һ��Ҫ�ڼ����Ȼ���֮����룬��BC��ȷ����5������150mL����Һ����Ҫ150mL������ƿ��������ƿ������ҺҪ�ò�����������������ƽ�ľ���Ϊ0��1g����A����ϴ��Һ��Ҫת�Ƶ�����ƿ�У���B��������ʹ��Һ���ƫ��Ũ��ƫС����C��ȷ��ҡ�Ⱥ��ã����ܼ�ˮ����D����
���㣺���⿼�黯ѧ��Ӧ�е������仯��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�人�и߶���ѧ������������ѧ�Ծ��������棩 ���ͣ������
��10�֣�1000��ʱ�������ƿ�������������Ӧ: Na2SO4(s)��4H2(g)  Na2S(s)��4H2O(g)����ش��������⣺
Na2S(s)��4H2O(g)����ش��������⣺
 ��1��������Ӧ��ƽ�ⳣ������ʽΪ�� ��
��1��������Ӧ��ƽ�ⳣ������ʽΪ�� ��
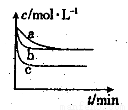
��2��������Ӧ��������ͬ�����½��У�������a�Ƚϣ�b��c�ֱ���ı�һ�ַ�Ӧ����������H2��Ũ����ʱ��ı仯��ͼ��ʾ��
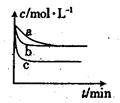
��������b�ı������Ϊ
�ڸ÷�Ӧ�ġ�H___0�����������������������
��3�����¶��£���2 Lʢ��1.42 g Na2SO4���ܱպ���������ͨ��H2��5 min
���ù�������Ϊ1.10 g��
�����ʱ�䷶Χ�ڵ�ƽ����Ӧ����v(H2)�� ��
����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ������ĸ����ͬ����
A��������ѹǿ���ֲ��� B�������������ܶȱ��ֲ���
C��c (H2)��c (H2O) D��v��(H2)��v��(H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
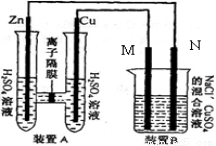
��4�֣���ͼװ��B����Ũ�Ⱦ�Ϊ0.1mol/L��NaCl��CuSO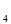 �����Һ����Һ���Ϊ500ml��M��N��Ϊʯī�缫����װ��A��Zn����������6.5gʱ��N����������____________g����ʱ�����е缫���ܹ��ռ���������������Ϊ___________L������ɱ�״���µ��������
�����Һ����Һ���Ϊ500ml��M��N��Ϊʯī�缫����װ��A��Zn����������6.5gʱ��N����������____________g����ʱ�����е缫���ܹ��ռ���������������Ϊ___________L������ɱ�״���µ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪298 Kʱ���ϳɰ���ӦN2(g)��3H2(g)  2NH3(g) ��H����92��0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ,��÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ):
2NH3(g) ��H����92��0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ,��÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ):
A��һ������92��0 kJ B����ȷ��
C��һ��С��92��0 kJ/mol D��һ��С��92��0 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڻ�ѧ��Դ��˵������ȷ���ǣ�
A�����ǿ��Ը��������ܶȵĴ�С���ж�Ǧ�����Ƿ���Ҫ��磻
B��ȼ�ϵ��������ȼ�Ϻ�������֮���������ԭ��Ӧ������ѧ��ת��Ϊ���ܣ�Ȼ����ת��Ϊ���ܵĻ�ѧ��Դ��
C����ͨп�̸ɵ���У�����������ԭ��Ӧ�����ʴֱ����ĺͲ�����ʹ���ˡ�
D����Ag2O��Zn�γɵļ�����пŦ�۵�أ������绯ѧ��Ӧʱ��Zn��Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(8��)�����¼������ʢ������Ȼ��Ƣ�Һ̬�Ȼ����Cu�����Ǣ�KAl��SO4��2��NaHCO3��Һ����ջش𣺣�����ţ�
��1���������������ڵ���ʵ��� �� ���ڷǵ���ʵ��� ���ܵ������ ��
��2��д���ݵĵ��뷽��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A��ͬ��ͬѹ�£���ͬ��������壬�������һ����ȣ�ԭ����Ҳһ�����
B���κ������£������ʵ����ļ���(CH4)��һ����̼�����һ����ͬ
C��ͬ��ͬѹ�µ�һ����̼����͵������������ȣ�������һ�����
D��50 mL 12 mol?L-1 Ũ�����������������̼��ȷ�Ӧ��ת�Ƶ�����Ϊ0��3 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��ӱ�ʡ������һ�С�������и߶���ѧ������������ѧ�Ծ��������棩 ���ͣ������
��9�֣���ѧ��Ӧ���ʱ�ͨ����ʵ����вⶨ��Ҳ�ɽ����������㡣
��1��ʵ���ã�5 g�״�(CH3OH��Һ̬)�������г��ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷų�113.5 kJ����������д���״�ȼ�յ��Ȼ�ѧ����ʽ�� ��
��2����֪��ѧ���ļ���Ϊ��
��ѧ�� | H��H | N��H |
|
����/( kJ��mol-1) | 436 | 391 | 945 |
��֪��ӦN2(g)+3H2(g)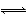 2NH3(g) ��H=a kJ��mol-1���Ը��ݱ������м������ݹ���a��ֵΪ ��
2NH3(g) ��H=a kJ��mol-1���Ը��ݱ������м������ݹ���a��ֵΪ ��
��3����֪��C(ʯī��s)+O2(g) CO2(g) ��H=-393 kJ��mol-1
CO2(g) ��H=-393 kJ��mol-1
2H2(g)+O2(g) 2H2O(l) ��H=-571.6 kJ��mol-1
2H2O(l) ��H=-571.6 kJ��mol-1
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ��H=-2599 kJ��mol-1
4CO2(g)+2H2O(l) ��H=-2599 kJ��mol-1
���ݸ�˹���ɣ�����298 KʱC(ʯī��s)��H2(g)��Ӧ����1 mol C2H2(g)���ʱ�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��ӱ�ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������װ��˵����ȷ����

A��װ�â��У������е�K������ZnSO4��Һ
B����װ�â۾���ͭʱ��c��Ϊ��ͭ
C��װ�âڹ���һ��ʱ���a��������Һ��pH����
D��װ�â� �е�����Zn����Fe��װ������Fe2������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com