
共轭双烯与含有双键的化合物相互作用,能生成六元环状化合物,常用于有机合成,例如:
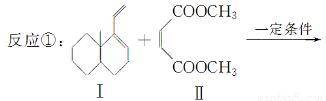
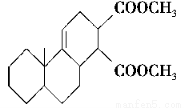
化合物Ⅱ可发生以下反应:
Ⅱ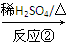 Ⅲ(分子式为C4H4O4)
Ⅲ(分子式为C4H4O4) 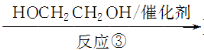 Ⅳ(高分子化合物)
Ⅳ(高分子化合物)
(1)化合物I的分子式为________,1 mol该物质完全燃烧需消耗________mol O2。
(2)反应②的化学方程式为__________________________________________。
(3)反应③是缩聚反应,化合物Ⅳ的结构简式为________。
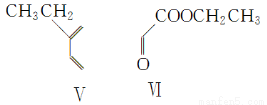
(4)在一定条件下,化合物Ⅴ和化合物Ⅵ能发生类似反应①的反应,生成两种化合物(互为同分异构体),这两种化合物的结构简式分别为________、________。
(5)下列关于化合物Ⅰ、Ⅱ、Ⅴ、Ⅵ的说法正确的有________(填字母)。
A.Ⅰ属于芳香烃
B.Ⅰ、Ⅱ、Ⅴ均能使溴的四氯化碳溶液褪色
C.Ⅴ与足量H2加成后的产物是3-甲基戊烷
D.加热条件下Ⅵ能与新制Cu(OH)2反应生成红色沉淀
(1)C13H20 18


(5)BCD
【解析】(1)化合物Ⅰ中有13个碳原子、4个不饱和度,故其分子式为C13H20。1 mol该物质完全燃烧消耗O2的物质的量为(13+20/4)mol=18 mol。(2)化合物Ⅱ是酯类化合物,反应②是化合物Ⅱ在稀硫酸作用下发生的水解反应,生成羧酸(HOOC—CH=CH—COOH)和醇(CH3OH)。
(3)HOOC—CH=CH—COOH和HOCH2CH2OH发生缩聚反应,生成聚酯
 。
。
(4)考虑到化合物Ⅴ和Ⅵ的结构不对称,所以二者发生反应时,可能生成两种产物。(5)化合物Ⅰ中不含苯环,不属于芳香烃,A错误。Ⅰ、Ⅱ、Ⅴ中均含有碳碳双键,均能使溴的四氯化碳溶液褪色,B正确。根据有机物传统命名法可知化合物Ⅴ与H2发生加成反应后的产物的名称为3-甲基戊烷,C正确。化合物Ⅵ中含有醛基,加热条件下能与新制Cu(OH)2反应生成红色沉淀,D正确。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源:2014年高中化学二轮创新训练上 专题8电化学原理练习卷(解析版) 题型:选择题
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示。则下列说法正确的是 ( )。
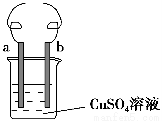
A.构成原电池时b极反应为Cu-2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b极质量可能减少也可能增加
D.构成的原电池或电解池工作后可能产生大量气体
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题4物质结构与元素周期律练习卷(解析版) 题型:选择题
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z位于同一主族,三种元素可以形成原子个数比为1∶1∶1的化合物W。下列推测正确的是 ( )。
A.元素Z的氧化物一定属于碱性氧化物
B.原子半径:X<Y<Z
C.三种元素中,Y的金属性最强
D.Y、Z都能形成含氧酸,且前者的酸性比后者强
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题2常用化学计量-物质的量练习卷(解析版) 题型:选择题
下列叙述正确的是( )。
A.1 mol·L-1 NaCl溶液含有NA个Na+
B.10 mL质量分数为98%的H2SO4用水稀释至100 mL,H2SO4的质量分数应大于9.8%
C.配制240 mL 1 mol·L-1的NaOH溶液需称NaOH固体的质量为9.6 g
D.配制1 mol·L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题2常用化学计量-物质的量练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法不正确的是( )。
A.1.5 mol NO2与足量的H2O反应,转移的电子数为NA
B.常温常压下,0.5NA个CO2分子质量为22 g
C.28 g氮气所含的原子数目为NA
D.在标准状况下,0.5NA个氯气分子所占体积是11.2 L
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题14物质结构与性质选考练习卷(解析版) 题型:填空题
元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等。这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用。请回答下列问题:
(1)N4分子是一种不稳定的多氮分子,这种物质分解后能产生无毒的氮气并释放出大量能量,能被应用于制造推进剂或炸药。N4是由四个氮原子组成的氮单质,其中氮原子采用的轨道杂化方式为sp3,该分子的空间构型为________,N—N键的键角为________。
(2)基态砷原子的最外层电子排布式为________。
(3)电负性是用来表示两个不同原子形成化学键时吸引键合电子能力的相对强弱,是元素的原子在分子中吸引共用电子对的能力。由此判断N、P、As、Sb的电负性从大到小的顺序是______________。
(4)联氨(N2H4)可以表示为H2N—NH2,其中氮原子采用的轨道杂化方式为________,联氨的碱性比氨的碱性________(填“强”或“弱”),其原因是________________________________________________________________。
写出N2H4与N2O4反应的化学方程式:____________________。
(5)元素X与N同周期,且X的原子半径是该周期主族元素原子半径中最小的,X与Ca形成的化合物CaX2的晶胞结构如图所示:
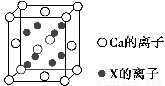
CaX2的晶体类型是________,一个晶胞中含有Ca的离子数为________,含有X的离子数为________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题13化学实验综合应用练习卷(解析版) 题型:实验题
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与硫酸反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定,以下实验过程不完整,请补充完整。

(1)按上图组装仪器,并______________________________________________;
(2)将8.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
(3)从左端导气管口处不断地缓缓通入H2,____________________________,
点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,________________________________________;
(5)测得反应后装置B增重2.25 g,则铁矿石中氧的百分含量为________。
Ⅱ.铁矿石中含铁量的测定,流程如下。
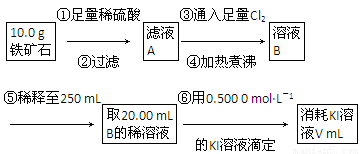
(1)步骤④中煮沸的作用是___________________________________________。
(2)步骤⑤中用到的玻璃仪器有烧杯、胶头滴管、250 mL容量瓶、________。
(3)下列有关步骤⑥的操作中说法正确的是________。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.锥形瓶不需要用待测液润洗
c.滴定过程中可利用淀粉溶液作指示剂
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
f.滴定结束后,滴定管尖嘴部分有气泡,则测定结果偏大
(4)若滴定过程中消耗0.500 0 mol·L-1 KI溶液20.00 mL,则铁矿石中铁的百分含量为________。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题12化学实验基础练习卷(解析版) 题型:选择题
在实验室中进行下列实验探究,其中的实验用品均能用到且正确的是 ( )。
选项实验探究内容实验用品
A铜丝在氯气中燃烧坩埚钳、燃烧匙、氯气、铜丝
B铝热反应铁架台、大蒸发皿、普通漏斗、铝粉、Fe2O3
C实验室制备氨气试管、集气瓶、酒精灯、NH4Cl、Ca(OH)2
D用KMnO4晶体配制500 mL 0.1 mol·L-1 KMnO4溶液容量瓶、烧杯、玻璃棒、酸式滴定管、KMnO4
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 4-2资源综合利用、环境保护练习卷(解析版) 题型:选择题
下列说法中不正确的是( )
A.与煤、石油相比较,天然气是一种比较清洁的化石燃料
B.乙醇是一种可再生能源,作为燃料的优点是完全燃烧的产物不污染环境
C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
D.煤转化为水煤气再燃烧放出的热量不会增加,因此煤的气化毫无意义
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com