
分析 由题给的条件可知,X、Y、Z、M、W这五种短周期元素的排列,不是按原子序数依次递增排列的,其中只有X、Y、Z三种元素是原子序数依次递增的同周期元素,由X、Y、Z的最外层电子数之和为15,最外层电子数平均为5,X与Z可形成XZ2气态分子,X为+4价,Y为-2价,可推出X、Y、Z分别为C、N、O三种元素;Y与M形成的气态化合物在标准状况下的密度0.76g•L-1,则该气态化合物的摩尔质量为22.4L/mol×0.76g•L-1=17g/mol,从而确定M为H元素;W的质子数是X、Y、Z、M四种元素质子数之和的一半,推出W的质子数为$\frac{1}{2}$×(6+7+8+1)=11,所以W为Na元素.
解答 解:由题给的条件可知,X、Y、Z、M、W这五种短周期元素的排列,不是按原子序数依次递增排列的,其中只有X、Y、Z三种元素是原子序数依次递增的同周期元素,由X、Y、Z的最外层电子数之和为15,最外层电子数平均为5,X与Z可形成XZ2气态分子,X为+4价,Y为-2价,可推出X、Y、Z分别为C、N、O三种元素;Y与M形成的气态化合物在标准状况下的密度0.76g•L-1,则该气态化合物的摩尔质量为22.4L/mol×0.76g•L-1=17g/mol,从而确定M为H元素;W的质子数是X、Y、Z、M四种元素质子数之和的一半,推出W的质子数为$\frac{1}{2}$×(6+7+8+1)=11,所以W为Na元素.
(1)CO2的结构式为O﹦C﹦O,故答案为:O﹦C﹦O;
(2)Y与M形成的气态化合物的摩尔质量为:17g/mol,故答案为:17g/mol;
(3)一种由X、Y、Z、M四种元素形成的离子化合物的化学式:(NH4)2CO3、NH4HCO3等,
故答案为:(NH4)2CO3、NH4HCO3等;
(4)M、W形成化合物为NaH,与水反应的化学方程式:NaH+H2O=NaOH+H2↑,
故答案为:NaH+H2O=NaOH+H2↑.
点评 本题以元素与物质推断为基础,综合考查原子结构、元素周期表、分子结构、元素化合物性质等知识,推断元素是解题关键,注意抓住短周期元素,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙酸丁酯 | B. | 甲酸乙酯 | C. | 乙酸甲酯 | D. | 乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
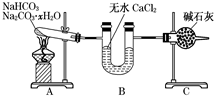 NaHCO3和Na2CO3•xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量).
NaHCO3和Na2CO3•xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂与还原剂的物质的量之比为1:4 | |
| B. | O2F2既是氧化剂又是还原剂 | |
| C. | 若生成4.48 L HF,则转移0.8 mol电子 | |
| D. | 氧气是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 类别 | 编号 |
| 新能源 | |
| 常规能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Ba2+、Cl-、NO3- | B. | K+、OH-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成a mol A的同时消耗2a mol C | |
| B. | 混合气体的压强不再变化 | |
| C. | 单位时间内消耗a mol A的同时消耗a mol B | |
| D. | B气体的浓度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 洗净的容量瓶中残留少量的蒸馏水 | B. | 溶解NaOH的烧杯未洗净 | ||
| C. | 称量NaOH时使用称量纸 | D. | 定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | |
| B. | 中性溶液中:Fe3+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中:Na+、ClO-、SO42-、I- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com