
| A、1mol任何物质所含的分子数均为NA |
| B、14g氮气所含的氮原子数为NA |
| C、标准状况下,22.4L水所含的水分子数为NA |
| D、在钠与氯气的反应中,1mol钠失去电子的数目为2NA |
| 14g |
| 14g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、与生铁相比纯铁更容易被腐蚀 |
| C、金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D、金属腐蚀的本质是M-ne?=Mn+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
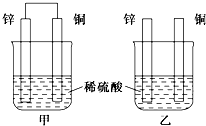 将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化产物只有H2S04 |
| B、1mol As2S3发生反应,有28 mol电子转移 |
| C、该反应中As2S3既是氧化剂又是还原剂 |
| D、As2S3不可能与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
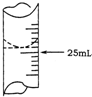 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).| 实验序号 | 待测NaOH溶液的体积/mL | HCl标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 20.10 |
| 2 | 25.00 | 1.50 | 21.40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com