
 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. _.
_. CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B. CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3
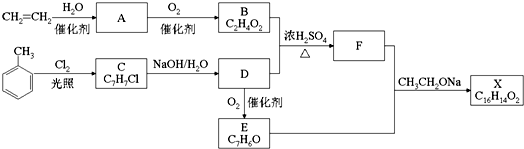
COOCH2CH2CH3分析 乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,则C为 ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为 ,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为
,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为 ,据此推断得出F为:
,据此推断得出F为: ,那么X为
,那么X为 ,据此结合各小题回答即可.
,据此结合各小题回答即可.
解答 解:乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,则C为 ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为 ,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为
,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为 ,据此推断得出F为:
,据此推断得出F为: ,那么X为
,那么X为 ,
,
(1)依据分析可知:B是乙酸,含有官能团为羧基,
故答案为:羧基;
(2)D为苯甲醇,D发生氧化反应得E,化学反应方程式为:2 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O,
+2H2O,
故答案为:2 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O;
+2H2O;
(3)依据分析可知,X为 ,
,
故答案为: ;
;
(4)X为 ,
,
A.X中不含有醛基,有与新制的Cu(OH)2悬浊液能发生反应,故A错误;
B.X中含有苯环,能与浓硝酸发生取代反应,故B正确;
C.X中含有碳碳双键,能使酸性KMnO4溶液褪色,故C正确;
D.X中含有酯基,能发生水解反应,故D错误;
故选BC;
(5)F为 ,分子式为:C9H10O2,
,分子式为:C9H10O2,
A、C中含有10个碳原子数,与F不是同分异构体,故A错误;
B中含有11个碳原子数,与F不是同分异构体,故B错误;
D的分子式均为C9H10O2,且与F结构不同,属于同分异构体,故D正确,
故选D.
点评 本题主要考查的是有机物的合成与有机物的推断,充分掌握常见有机化合物的性质以及抓住所给信息解题是关键,有一定的难度,注意整理.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaH中H的化合价为-1价 | B. | H2O既不是氧化剂也不是还原剂 | ||
| C. | 该反应的离子方程式为:H-+H+═H2↑ | D. | NaOH是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应不一定伴随着能量的变化 | |
| B. | 氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=571.6kJ•mol-1 | |
| C. | 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 | |
| D. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y 型管和止水夹分别接c.d 两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是( )
如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y 型管和止水夹分别接c.d 两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是( )| A. | 饱和NaHCO3 溶液、12mol•L-1盐酸、18.4mol•L-1H2SO4 | |
| B. | 饱和Na2CO3 溶液、2mol•L-1 H2SO4、饱和NaOH 溶液 | |
| C. | 饱和NaOH 溶液、2mol•L-1 H2SO4、18.4mol•L-1H2SO4 | |
| D. | 18.4mol•L-1H2SO4、饱和NaOH 溶液、18.4mol•L-1H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某次酸雨的pH为4.3,是由于溶解了CO2 | |
| B. | 生铁、不锈钢、青铜都属于合金 | |
| C. | 汽车尾气不会引起呼吸道疾病 | |
| D. | 普通玻璃的主要成分是纯碱、石灰石和石英 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com