
(1)若5.2g乙炔(C2H2气态)完全燃烧生成液态水和CO2(g)时放热260kJ。该反应的热化学方程式为 ;
乙炔的燃烧热为 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
__________________________________________________________________________。
(3)已知:
2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1
则Al和FeO发生铝热反应的热化学方程式为:
__________________________________________________________
科目:高中化学 来源: 题型:
右图模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是
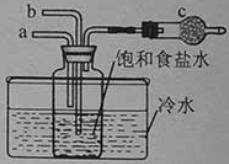
A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.按系统命名法,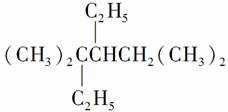 的名称为3,3,6三甲基4乙基庚烷
的名称为3,3,6三甲基4乙基庚烷
B.下图是某有机物分子的比例模型,该物质可能是一种氨基酸
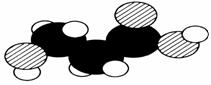
C.能用新制氢氧化铜和NaOH溶液鉴别甘油、葡萄糖溶液、乙酸钠溶液
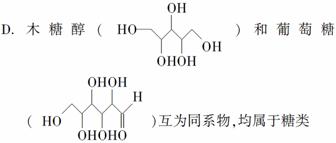
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃的混合物共1 L,在空气中完全燃烧得到1.5 L CO2和2 L水蒸气(体积均在同温同压下测定),关于此混合烃的判断正确的是 ( )
A.肯定是甲烷和乙烯的混合物 B.一定不是甲烷和乙烯的混合物
C.一定含乙烯,不含甲烷 D.两种烃分子中氢原子数都是4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列涉及有机物的说法正确的是( )
A.乙烯和聚乙烯都能发生加聚反应
B.汽油、煤油、柴油和植物油都是碳氢化合物
C.乙烯、苯都可与溴水发生加成反应
D.2己烯能使KMnO4(H+)溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
有关电化学知识的描述正确的是 ( )
A.CaO+H2O===Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能
B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液
C.原电池的两极一定是由活动性不同的两种金属组成
D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氢氧燃料电池以KOH溶液作电解质溶液时,工作一段时间后,电解质溶液的浓度将________,溶液的pH____________________________________________________。
(填“减小”、“增大”或“不变”)
(2)氢氧燃料电池以H2SO4溶液作电解质溶液时,工作一段时间后,电解质溶液的浓度将________,溶液的pH_____________________________________________________。
(填“减小”、“增大”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
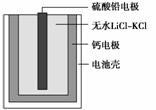
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本 结构如图所示,其中作为电解质的无水LiClKCl混合物受热熔融后,电池即可瞬间输出 电能。该电池总反应为PbSO4+2LiCl+Ca===CaCl2+Li2SO4+Pb。
下列有关说法正确的是 ( )
A.正极反应式:Ca+2Cl--2e-===CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1 mol电子,理论上生成20.7 g Pb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是稀硫酸与某金属反应的实验数据:
| 实验序号 | 金属质量 | 金属状态 | c(H2SO4) /mol·L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
分析上述数据,回答下列问题:
(1)实验4和5表明,________________对反应速率有影响,______________反应速率越快,能表明同一规律的实验还有__________(填实验序号);
(2)实验1、3、4、6、8表明反应物浓度对反应速率产生影响,能表明同一规律的实验还有______________(填实验序号);
(3)本实验中影响反应速率的其他因素还有________,其实验序号是6和________,8和__________。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com