

分析 (1)氨气的催化氧化化学方程式;
(2)吸收塔C中通入空气的目的是将一氧化氮氧化成二氧化氮;根据反应中各物质的组成元素的化合价是否发生变化来判断是否发生氧化还原反应;
(3)铜与浓硝酸反应生成硝酸铜、二氧化氮和水,反应中Cu被氧化,N元素被还原;,根据n=$\frac{m}{M}$结合1molCu转移电子数为2mol解答.
解答 解:(1)B中氨气转化为NO的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)在整个生产流程中,吸收塔C中通入空气的目的是将一氧化氮氧化成二氧化氮;题中涉及的化学反应有:A、N2+3H2?2NH3,B、4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O,C、2NO+O2═2NO2、3NO2+H2O═2HNO3+NO、4NO2+O2+H2O═4HNO3,D、NH3+HNO3═NH4NO3,其中A、B、C属于氧化还原反应,
故答案为:将一氧化氮氧化成二氧化氮;ABC;
(3)铜与浓硝酸反应生成硝酸铜、二氧化氮和水,反应的离子方程式为Cu+4H++2NO3-═Cu2++2H2O+NO2↑,1molCu转移电子数为2mol,25.6gCu的物质的量为:$\frac{25.6g}{64g/mol}$=0.4mol,转移0.8mol电子,
故答案为:Cu+4H++2NO3-═Cu2++2H2O+NO2↑;0.8.
点评 本题考查了氮及其化合物性质、氧化还原反应等,题目难度中等,注意氮的氧化物的性质是高频考点,侧重考查学生分析思维能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空:
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

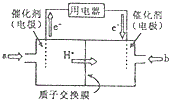
| A. | 燃料电池工作时,负极反应为:H2-2e-=2H+ | |
| B. | 若要实现铁上镀铜,则a极是铁,b极是铜 | |
| C. | 若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | a、b两极均是石墨时,在相同条件下当电池中消耗H2 22.4 L(标准状况)时,a极析出铜64 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2,CH4,O2等均是温室效应的气体 | |
| B. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| C. | 磁共振谱可以鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c>b>d>a | B. | b>a>d>c | C. | a>d>b>c | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙酸(乙酸钠、水):加入硫酸,后结晶、过滤 | |
| B. | 乙酸乙酯(乙酸):加入饱和碳酸钠溶液,后分液 | |
| C. | 苯(苯酚):加入浓溴水,后过滤 | |
| D. | 氢氧化铁胶体(FeCl3):渗析 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3通入水中:SO3+H2O═H2SO4 | |
| B. | Cl2通入FeCl2溶液中:Cl2+2FeCl2═2FeCl3 | |
| C. | HCl气体通入NaOH溶液中:HCl+NaOH═NaCl+H2O | |
| D. | CO2通入NaOH溶液中:CO2+2NaOH═Na2CO3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com