
【题目】温度为T时.向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5 (g)![]() PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 在前50s,PCl3的平均反应速率 v(PCl3)=0.0032mol/(L·s)
B. 达到平衡时,容器中的压强是起始时的1.2倍
C. 相同温度下,起始时向容器中充入1.0mo PCl5、0.20 mo1 PCl3和0.20 mo1 Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
【答案】BC
【解析】A.由表中数据可知,50s内△c(PCl3)=0.16mol÷2L=0.08mol/L,v(PCl3)=0.08mol/L÷50s=0.0016mol/(Ls),A错误;B.由表中数据可知,平衡时n(PCl3)=0.2mol,生成氯气也是0.2mol,剩余PCl5是0.8mol,所以达到平衡时,容器中的压强是起始时的1.2mol/1.0mol=1.2倍,B正确;C.根据方程式可知
PCl5 (g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
开始(mol/L):0.5 0 0
变化(mol/L):0.1 0.1 0.1
平衡(mol/L):0.4 0.1 0.1
所以平衡常数K=0.1×0.1/0.4=0.025;起始时向容器中充入1.0mo PCl5、0.20 mo1 PCl3和0.20 mo1 Cl2,起始时PCl5的浓度为0.5mol/L、PCl3的浓度为0.1mol/L、Cl2的浓度为0.1mol/L,浓度商Qc=0.1×0.1/0.5=0.02<K=0.25,说明平衡向正反应方向移动,反应达平衡前v(正)>v(逆),C正确;D.等效为起始加入2.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动,平衡时的PCl5转化率较原平衡低,故平衡时PCl3的物质的量小于0.4mol,即相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的物质的量小于0.4mol,参加反应的PCl3的物质的量大于1.6mol,故达到平衡时,PCl3的转化率高于1.6mol/2mol=80%,D错误,答案选BC。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在3Cl2+8NH3=6NH4Cl+N2反应中,以下说法不正确的是
A. 还原剂是NH3 ,
B. 该反应中每生成1mol N2则转移的电子数为6NA
C. 氧化性大小顺序为:Cl2> N2
D. Cl2和NH3都可以用碱石灰来干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着卤素原子半径的增大,下列递变规律正确的是( )
A. 单质的熔、沸点逐渐降低 B. 卤素离子的还原性逐渐增强
C. 单质的氧化性逐渐增强 D. 气态氢化物的稳定性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )。
A. 每一周期的元素都是从碱金属开始,最后以稀有气体结束
B. 同一周期中(除第一周期外),从左到右,各元素原子核外电子数都是从1逐渐增加到8
C. 第二、三周期上下相邻元素的原子核外电子数相差8
D. 第七周期排满后只有23种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据新华社消息,卫生部拟从2011年12月1日起,禁止在面粉生产中使用过氧化苯甲酰和过氧化钙。过氧化苯甲酰的结构简式如图所示。

(1)过氧化苯甲酰的分子式为________,其一氯代物共有________种。
(2)工业上可以利用苯甲酰氯(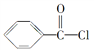 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:___________________,该反应属于________反应。
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:___________________,该反应属于________反应。
(3)过氧化苯甲酰用于面粉漂白后会产生苯甲酸:
![]()
![]() 。
。
苯甲酸的同分异构体中,属于酯类的有__________,属于酚类的有_________________ (写结构简式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。已知室温下:Ka(CH3COOH)=1.7×10-5 mol·L-1;H2CO3的电离常数Ka1=4.2×10-7mol·L-1、Ka2=5.6×10-11mol·L-1。
(1)①请用离子方程式解释碳酸氢钠水溶液显碱性的原因________________。
②常温下,物质的量浓度相同的下列四种溶液:a、碳酸钠溶液 b、醋酸钠溶液 c、氢氧化钠溶液 d、氢氧化钡溶液。其pH由大到小的顺序是:_____(填序号)。
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是_______;该醋酸溶液稀释过程中,下列各量一定变小的是______________。

a.c(H+) b.c(OH-)
c.![]() d.
d.![]()
(3)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw=___________mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH= _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于容量瓶及其使用方法的叙述正确的是( )。
①容量瓶是配制一定物质的量浓度的溶液的专用仪器 ②容量瓶使用前要先检查容量瓶是否漏液 ③容量瓶可以用来加热 ④容量瓶不能用长期贮存配制好的溶液 ⑤一定要用500mL容量瓶配制250mL溶液
A. ①③ B. ①②④⑤ C. ①②④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2![]() 2AlON+CO合成,下列有关说法正确的是( )
2AlON+CO合成,下列有关说法正确的是( )
A. 氮氧化铝中氮的化合价是-3
B. 反应中氧化产物和还原产物的物质的量之比是1∶2
C. 反应中每生成5.7 g AlON同时生成1.12 L CO
D. AlON和CO的化学键类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液与30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g/cm3的混合溶液.计算:
(1)混合后溶液的质量分数。
(2)混合后溶液的物质的量浓度。
(3)在1 000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com