
【题目】12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________,R的相对原子质量为________。
科目:高中化学 来源: 题型:
【题目】烃分子中若含有双键,叁键或环,其碳原子所结合的氢原子则少于同碳原子数对应烷烃所含的氢原子数,亦具有一定的不饱和度(用W表示)。下表列出几种烃的不饱和度:
有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
W | 1 | 2 | 1 | 4 |
据此下列说法不正确的是
A. 1molW=3的不饱和链烃再结合6molH即达到饱和
B. ![]() 的W等于6
的W等于6
C. CH3CH2CH=CH2与环丁烷的不饱和度相同
D. C4H8的不饱和度与C3H6、C2H4的不饱和度不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)已知某反应中能量变化如图所示,所得结论错误的是( )

A. 该图像可以表示氯化铵与消石灰反应的能量变化
B. 该反应过程中,一定有其他形式的能量转化成化学能
C. 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量
D. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才可进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为2L的密闭容器中充入2mol X,一定条件下可发生反应:2X(g)![]() 3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知
3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知![]() min时容器内有1.5mol Y。下列叙述正确的是( )
min时容器内有1.5mol Y。下列叙述正确的是( )

A. 若![]() min时升高温度,则反应速率不变
min时升高温度,则反应速率不变
B. ![]() ~
~![]() min内,
min内,![]() ,反应不再发生
,反应不再发生
C. 0~![]() min内,
min内,![]()
D. ![]() min时,只有正反应发生
min时,只有正反应发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当前能源危机是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法有利于能源“开源节流”的是________(填字母)。
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
D.减少资源消耗,加大资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=________。

(3)已知:N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。N2(g)+O2(g)=2NO(g) ΔH=+180kJ/mol。NO分子中化学键的键能为__________________kJ/mol。
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:________________。
(5)已知Na2SO4·10H2O![]() Na2SO4·nH2O+(10-n)H2O。将装有芒硝(Na2SO4·10H2O)的密闭聚乙烯管安装在房屋的外墙内就能达到白天蓄热,使室内保持较低温度,晚上把白天所蓄的热量放出,使室内保持温暖的目的。则白天和晚上的能量转化方式是白天将________能转化为________能,晚上将________能转化为________能。
Na2SO4·nH2O+(10-n)H2O。将装有芒硝(Na2SO4·10H2O)的密闭聚乙烯管安装在房屋的外墙内就能达到白天蓄热,使室内保持较低温度,晚上把白天所蓄的热量放出,使室内保持温暖的目的。则白天和晚上的能量转化方式是白天将________能转化为________能,晚上将________能转化为________能。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_________________。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:
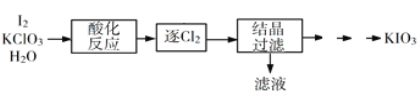
“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是______________________。
“滤液”中的溶质主要是__________________。
(3)KIO3也可采用“电解法”制备,装置如图所示。
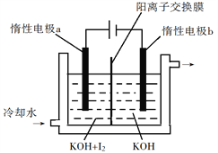
①写出电解时阴极的电极反应式________________________________。
②电解过程中通过阳离子交换膜的离子主要为_______________。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有___________________________________________(写出一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成离子化合物,其阴阳离子个数比为1∶1。回答下列问题:
(1)五种元素中非金属性最强的是_______________(填元素符号)。
(2)由A和B、D、E所形成的共价化合物中,热稳定性最差的是___________(用化学式表示)。
(3)C和E形成的离子化合物的电子式为 ______ ,用电子式表示A和B形成的过程_____,A和E形成的化合物与A和B形成的化合物反应,产物的化学式为_______________
(4)D的最高价氧化物的水化物的化学式为____________________。
(5)由A和B形成的一种气体在工业上用途很广,实验室制取的方程式为____________________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________。
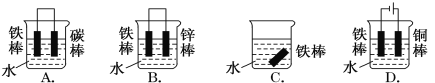
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
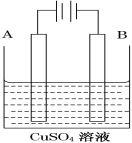
①A电极对应的金属是________(写元素名称),
B电极的电极反应式是___________________________________。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________mol。
③镀层破损后,不易被腐蚀的是___________(填A或B)。
A.镀铜铁 B.镀锌铁 C. 镀锡铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com