
(1)实验室制取 的反应为___________________________________.
的反应为___________________________________.
(2)其装置与实验室制__________________________________装置相同.
(3) 一般用______方法收集,教材中的收集装置里棉花的作用是______________.
一般用______方法收集,教材中的收集装置里棉花的作用是______________.
(4)检验 收集满的常用方法有_______________________________.
收集满的常用方法有_______________________________.
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:阅读理解
| 元素 | 有关信息 |
| X | 元素主要化合价-2,原子半径为0.0074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
| D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
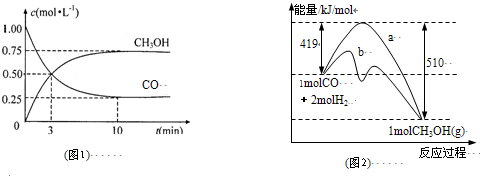
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| n(CH3OH) |
| n(CO) |
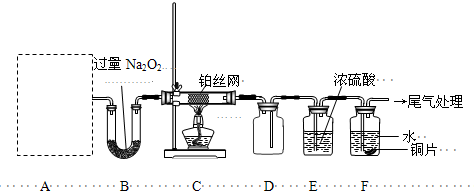

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室制取乙烯的反应原理为CH3CH2OH
实验室制取乙烯的反应原理为CH3CH2OH
| ||
| 170℃ |
查看答案和解析>>
科目:高中化学 来源:湖南省澧县一中、岳阳县一中2012届高三11月联考化学试题 题型:058
纯净的NO是无色气体,很容易与许多分子发生反应.在有生命的有机体中会不断地产生NO,并被用来在细胞内和细胞间传递信息.它还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.试回答下列问题:
(1)实验室制取NO的化学方程式:________.
(2)收集NO气体应采用________法,若采用此法收集NO气体,应从装置A的________端进气(填“a”或者“b”).
(3)甲同学用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图:
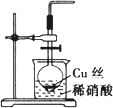
打开分液漏斗的活塞使反成进行,能否制得纯净的NO气体?________(填“能”或者“不能”);若不能,原因是________(用化学方程式表示).
(4)为证明铜丝与稀硝酸反应生成的是NO,乙同学另设计了一套制取NO的装置,如图:
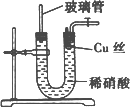
①让反应停下的操作是________;
②长玻璃管的作用是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com