
对于1L 0.1 mol·L-1 NH4Cl溶液,正确的是
A.溶液呈碱性
B.通入少量HCl,c(NH4+)和c(Cl-)均增大
C.溶液中含有NH4+数目为0.1NA(NA表示阿伏加德罗常数的数值)
D.升高温度,溶液pH升高
科目:高中化学 来源:2014秋江苏省东台市高二第一学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质中,一定互为同系物的是
A.C4H10和C20H42
B.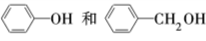
C.C4H8和C3H6
D.一溴乙烷和1,2—二溴乙烷
查看答案和解析>>
科目:高中化学 来源:2014秋广东省揭阳市高二第一学期期中考试化学试卷(解析版) 题型:选择题
在酸性溶液中,下列各组离子能大量共存的是
A.Cl-、HCO3-、K+、SO42- B.OH-、Cl-、Na+、Mg2+
C.Fe3+、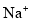 、SO32-、I- D.Na+、Cl-、I-、SO42-
、SO32-、I- D.Na+、Cl-、I-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(理)化学试卷(解析版) 题型:填空题
(10分)
甲醇是一种重要的化工原料。
(1)已知:① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l)= H2O(g) △H=+ 44.0 kJ·mol—1
写出表示甲醇燃烧热的热化学方程式 。
(2)甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。其反应为:
CH3OH (g)+ H2O (g) CO2(g) +3H2 (g) △H=-72.0kJ/mol
CO2(g) +3H2 (g) △H=-72.0kJ/mol
①该反应的平衡常数表达式为__________________。
②下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.恒容再充入1molH2O(g)
(3)甲醇可以氧化成甲酸,在常温下用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH) _________ (填“<”或“>”或“=”) 20. 00 mL。
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(理)化学试卷(解析版) 题型:选择题
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4 B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③ D.N2的转化率:②>①>③
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(理)化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应
B.增大压强是通过提高活化分子的百分数来提高反应速率
C.氮的固定只有在高温、高压、催化剂的条件下才能实现
D.水煤气是可再生能源
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(文)化学试卷(解析版) 题型:选择题
下列说法中,不正确的是
A.钠、钾着火时可用水灭火
B.面粉厂或加油站不必严禁烟火
C.氨气泄漏时可喷洒大量水进行处理
D.皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(文)化学试卷(解析版) 题型:选择题
下列措施不能够使化学反应速率加快的是
A.升高温度 B.降低温度
C.使用催化剂 D.增大固体反应物面积
查看答案和解析>>
科目:高中化学 来源:2014秋广东省广州市高二上学期期中考试化学(理)试卷(解析版) 题型:填空题
(15分)
(一)对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。下表为几种弱酸在25℃时的电离平衡常数
酸 | 电离平衡常数K |
|
|
|
|
|
|
回答下列问题:
(1)K只与温度有关,当温度升高时,K值____(填“增大”、“减小”、“不变”)。
(2)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是_________,最弱的是________。
(3)对于同一种多元弱酸,有不止一个电离平衡常数,多个常数K1、K2、K3、之间存在某种大小关系,此关系是________________;以碳酸为例,用离子方程式和必要的文字说明产生此规律的原因_________________________。
(4)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的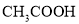 的电离转化率为____,则该温度下醋酸的电离平衡常数
的电离转化率为____,则该温度下醋酸的电离平衡常数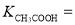 _____。
_____。
(二)化合物SOCl2是一种液态化合物,沸点77 ℃。在盛有10 mL水的锥形瓶中,小心地滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。该气体可使滴有品红试液的滤纸褪色。
(1)写出SOCl2和水反应的化学方程式:_____________________________。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是 ;用SOCl2与AlCl3·6H2O混合共热得到无水AlCl3,原因是________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com