
| A. | 向含有FeCl2的溶液中通入适量氯气,当有1molFe2+被氧化时,该反应转移电子数目为3NA | |
| B. | 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5NA | |
| C. | 含0.1molNH4HSO4的溶液中,阳离子数目略小于0.2NA | |
| D. | C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代,1mol此有机物所含共用电子对数目为13NA |
分析 A.有1molFe2+被氧化时生成1mol铁离子,转移了1mol电子;
B.CuO和Cu2S中铜的质量分数相同,据此计算出铜的质量及物质的量;
C.0.1molNH4HSO4中含有0.1mol硫酸根离子,带有负电荷为0.2mol,溶液中还含有氢氧根离子,则负电荷的总物质的量大于0.2mol,根据电荷守恒可知阳离子的物质的量大于0.2mol;
D.C3H8中含有10个共价键,氨基中含有2个共价键,羟基中含有1个共价键,则取代产物中含有13个共价键.
解答 解:A.向含有FeCl2的溶液中通入适量氯气,当有1molFe2+被氧化时会生成1mol铁离子,转移电子的物质的量为1mol,转移电子数目为NA,故A错误;
B.40gCuO和Cu2S混合物中含有Cu的物质的量为:$\frac{\frac{64}{80}×40g}{64g/mol}$=0.5mol,则所含铜原子的数目为0.5NA,故B错误;
C.含0.1molNH4HSO4的溶液中含有0.1molSO42-,0.1molSO42-带有0.2mol负电荷,由于溶液中还含有氢氧根离子,则负电荷的总物质的量大于0.2mol,根据电荷守恒,溶液中正电荷的总物质的量一定大于0.2mol,溶液中阳离子为铵根离子、氢离子,都大于1个单位正电荷,则溶液中含有阳离子数目略大于0.2NA,故C错误;
D.C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代,取代产物中含有的共用电子对与丙烷、氨基、羟基中总电子对数相同,C3H8分子中含有10个共价键、氨基中含有2个共价键、羟基中含有1个共价键,取代产物中含有13个共价键,则1mol此有机物含有13mol共用电子对,所含共用电子对数目为13NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,试题有利于提高学生灵活运用基础知识解决实际问题的能力.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶未干燥 | |
| B. | 定容时俯视液面 | |
| C. | 转移时有液体溅出 | |
| D. | 颠倒摇匀后发现液面低于刻度线,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
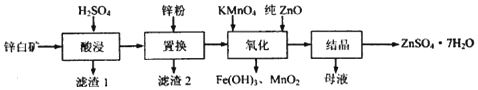
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 6.4 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
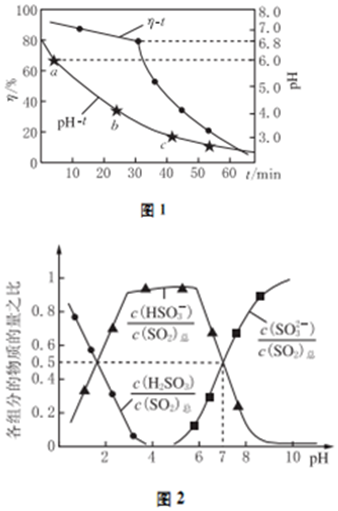
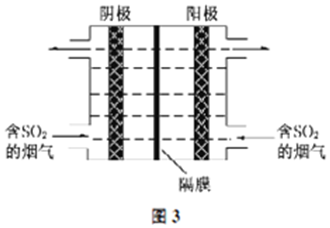
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 | 3 |
| 实验步骤 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于空气中,观察现象 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于氧气中,观察现象 | 取少量淀粉碘化钾溶液置于试管中,通往足量的氯气,观察现象 |
| 实验现象 | 试纸缓慢变蓝 | 试纸不变蓝 | 溶液先变蓝后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
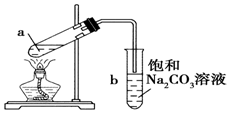
| A. | 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 | |
| B. | 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象 | |
| C. | 实验时加热试管a的目的是加快反应速率并及时将乙酸乙酯蒸出 | |
| D. | 试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com