
| A、通入H2S气体 |
| B、加水稀释 |
| C、加入AgNO3溶液 |
| D、加入NaBr溶液 |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
| A、①②③⑤ | B、①④⑤ |
| C、①②③ | D、②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
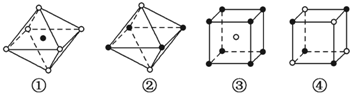
| A、①和③ | B、①和④ |
| C、只有③ | D、只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温、高压 |
| 催化剂 |
| A、92.4kJ?mol-1 |
| B、-92.46kJ?mol-1 |
| C、184.8 kJ?mol-1 |
| D、-184.8 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气的水溶液可以导电,说明氯气是电解质 |
| B、漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| C、氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 |
| D、为证明氯水中含Cl-,可先加盐酸酸化,再加入AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
| A、Na(s)与Cl2(g)反应生成1mol NaCl(s)放出的热量为556.1kJ |
| B、Si(s)+2Cl2(g)═SiCl4(g)△H=-602kJ?mol-1 |
| C、从表中可以看出,氯化钠的熔点比晶体硅高 |
| D、从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol H2完全燃烧生成液态水时放出571.6kJ的热量 | ||
| B、1mol H2完全燃烧生成液态水时放出285.8kJ的热量 | ||
| C、2个氢分子完全燃烧生成液态水时放出571.6 kJ的热量 | ||
D、上述热化学方程式可表示为H2(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①与a、b |
| B、②与a、b |
| C、③与a、c |
| D、②与a、d |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com