
水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图像,模型见图。下列关于水的说法正确的是( )

A.水是弱电解质
B.可燃冰是可以燃烧的水
C.氢氧两种元素只能组成水
D.0 ℃时冰的密度比液态水的密度大
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
最近科学家冶炼出了纯度高达99.999 9%的铁,据你推测,下列性质它不可能具有的是( )
A、硬度比生铁低
B、在潮湿空气中放置不易生锈
C、在冷的浓硫酸中可钝化
D、与4 mol·L-1盐酸反应的速率比生铁快
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子反应方程式为( )
A.NH4HCO3溶于过量的浓KOH溶液中:
NH + HCO
+ HCO +2OH-=== CO
+2OH-=== CO + NH3↑+2H2O
+ NH3↑+2H2O
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO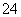 沉淀完全:2Al3++3SO
沉淀完全:2Al3++3SO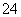 +3Ba2++
+3Ba2++
6OH-===2Al(OH)3↓+3BaSO4↓
C.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
D.醋酸除去水垢:2H++CaCO3===Ca2++ CO2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO ,其离子方程式为__________________________________________。
,其离子方程式为__________________________________________。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,________显正电性。BrCl与水发生反应的化学方程式为____________________________________________。
(3)CuBr2分解的热化学方程式为:
2CuBr2(s)===2CuBr(s)+ Br2(g)
ΔH=+105.4 kJ/mol
在密闭容器中将过量CuBr2于487 K下加热分解,平衡时p(Br2)为4.66×103 Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会________(填“增大”“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。

Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O +I2===S4O
+I2===S4O +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。

Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO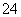 ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式不正确的是( )
A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH===Mg2++2CH3COO-+2H2O
B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO +3H2O2+6H+===2Mn2++6H2O+4O2↑
+3H2O2+6H+===2Mn2++6H2O+4O2↑
C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO +OH-===CaCO3↓+H2O
+OH-===CaCO3↓+H2O
D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO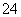 恰好沉淀完全:NH
恰好沉淀完全:NH +H++SO
+H++SO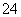 +Ba2++2OH-===NH3·H2O+BaSO4↓+H2O
+Ba2++2OH-===NH3·H2O+BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
“乙醇汽油”就是在汽油里加入适量的乙醇混合而成的一种燃料。下列有关叙述不正确的是( )
A.汽车使用乙醇汽油能减少有害气体的排放
B.工业上常用裂化的方法提高汽油的产量和质量
C.乙醇汽油是多种烃的混合物
D.用玉米、高粱发酵可以制得乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。右图为RFC工作原理示意图,有关说法正确的是
A.当有0.1 mol电子转移时,a极产生 0.56 L O2(标准状况下)
B.左端装置中化学能转化为电能,右端装置中电能转化为化学能
C.d极上发生的电极反应是:O2 + 4H+ + 4e- 2H2O
D.c极上进行还原反应,右端装置B中的H+可以通过隔膜进入A

查看答案和解析>>
科目:高中化学 来源: 题型:
下表中对应关系正确的是( )
| A | CH3CH3+Cl2 CH2===CH2+HCl―→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br-===2Cl-+Br2 Zn+Cu2+===Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O===4NaOH+O2↑ Cl2+H2O===HCl+HClO | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com