
| A. | 煤的干馏、石油分馏、石油裂解都是化学反应 | |
| B. | 煤经过气化、液化等化学变化可得到清洁燃料 | |
| C. | 人造纤维、合成纤维和油脂都是有机高分子化合物 | |
| D. | 棉花、羊毛、蚕丝、麻都由C、H、O元素构成 |
分析 A.石油分馏与物质的沸点有关;
B.煤气化生成CO和氢气、液化生成甲醇;
C.油脂的相对分子质量在10000以下;
D.羊毛、蚕丝的成分为蛋白质,含N元素.
解答 解:A.石油分馏与物质的沸点有关,为物理变化,而煤的干馏、石油裂解都是化学反应,故A错误;
B.煤气化生成CO和氢气、液化生成甲醇,均为化学变化可得到清洁燃料,故B正确;
C.油脂的相对分子质量在10000以下,不是高分子,而人造纤维、合成纤维都是有机高分子化合物,故C错误;
D.羊毛、蚕丝的成分为蛋白质,含N元素,而棉花、麻都由C、H、O元素构成,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机物的组成、有机反应为解答的关键,侧重分析与应用能力的考查,注意煤和石油的综合应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
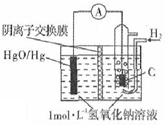 某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )
某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )| A. | 正极反应为:HgO(s)-2e-+H20=Hg(l)+2OH- | |
| B. | 放电结束后,溶液中的pH值下降 | |
| C. | 每反应2.24L氢气,交换膜通过0.2mol离子 | |
| D. | 电子通过离子交换膜从负极向正极移动,保持溶液中电荷平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N5 →5N2是化学变化 | B. | N5和N2互为同位素 | ||
| C. | 原子半径:r(N)<r(O) | D. | 18O2中含18个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{97}^{249}$Bk(锫)中的中子数为97 | |
| B. | ${\;}_{117}^{293}$UP和${\;}_{117}^{294}$UP互为同位素 | |
| C. | 用 ${\;}_{20}^{48}$Ca轰击${\;}_{97}^{249}$Bk的变化是化学变化 | |
| D. | ${\;}_{20}^{48}$Ca、${\;}_{97}^{249}$Bk、${\;}_{117}^{293}$UP、${\;}_{117}^{294}$UP属于四种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | 只有③ | C. | ③④⑤ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2中所含有的阴离子数目是0.2NA | |
| B. | 标准状况下,2.24L18O2中含有的中子的数目是NA | |
| C. | 在20℃、1.01×105 Pa时,2.8g C2H4和CO的混合气体含气体分子数是0.1 NA | |
| D. | 标准状况下,a L CH4和a L C6H14中所含分子数均约为$\frac{a{N}_{A}}{22.4}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com