
| A、2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1Na |
| B、1mol Na2CO3晶体中含CO32-离子数小于1 Na |
| C、惰性电极电解食盐水,若线路中通过1mol电子电量,则阳极产生气体11.2L |
| D、0.1 mol的CaC2中含阴离子数是2 Na |


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
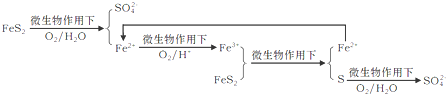
| O2/H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、Cl2>MnO2>I2 |
| B、MnO2>Cl2>I2 |
| C、I2>MnO2>Cl2 |
| D、I2>Cl2>MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| B、标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向盐酸中滴加氨水:H++OH-=H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O |
| D、CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所得的分散系属于悬浊液 |
| B、所得的分散系中分散质为Fe2O3 |
| C、该分散系能产生丁达尔效应 |
| D、所得分散系为胶体,且胶粒直径即为氢氧化铁分子直径 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某充电宝锂离子电池的总反应为:xLi+Li1-xMn2O4
某充电宝锂离子电池的总反应为:xLi+Li1-xMn2O4| 放电 |
| 充电 |
| 放电 |
| 充电 |
| A、锂离子电池放电时Li+向正极迁移 |
| B、镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-═Ni(OH)2+OH- |
| C、右图表示用锂离子电池给镍氢电池充电 |
| D、锂离子电池充电时,阴极的电极反应式:LiMn2O4-xe-═Li1-xMn2O4+xLi+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑥⑦ | B、③⑤⑧ |
| C、③⑦⑧ | D、③④⑥⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com