
| A. | CCl4 和NaCl | B. | I2和NaI | C. | SiO2和O2 | D. | CO2和H2O |
分析 根据晶体中微粒间的作用力分析,由离子键构成的晶体为离子晶体,微粒间以共价键结合形成的空间网状结构的晶体为原子晶体,微粒间以分子间作用力结合形成的晶体为分子晶体.
解答 解:A、NaCl是由离子键构成的晶体为离子晶体,CCl4是以分子间作用力结合形成的分子晶体,二者晶体类型不同,故A错误;
B、NaI是由离子键构成的晶体为离子晶体,I2是以分子间作用力结合形成的分子晶体,二者晶体类型不同,故B错误;
C、O2是以分子间作用力结合形成的分子晶体,SiO2是共价键结合的原子晶体,二者晶体类型不同,故C错误;
D、CO2和H2O是以分子间作用力结合形成的分子晶体,二者晶体类型相同,故D正确;
故选D.
点评 本题考查了晶体类型和化学键的关系的判断,题目难度不大,注意把握有关概念及晶体中微粒间的作用力.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | 如果XY2是共价化合物,则X与Y的原子序数不可能相差1 | |
| B. | 如果X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液 | |
| C. | 如果X与Y的原子序数相差5,则离子化合物XY2不溶于水 | |
| D. | 如果XY2是离子化合物,则X与Y的原子序数可能相差9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | B | a | C |
| A. | A-B+C | B. | 2C-A-B | C. | C-A-B | D. | A-B+2C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
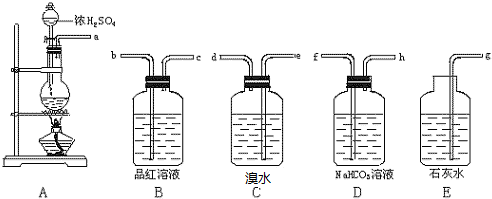
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | >7 | B. | <7 | C. | =7 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CHCl3只有一种结构 | |
| B. | CH2Cl2只有一种结构 | |
| C. | CH4是非极性分子 | |
| D. | CH4的四个价键的键长和键能都相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com