
【题目】某中学化学兴趣小组学生在学习“含硫化合物的性质和应用”时,进行了如下实验探究:为了验证浓硫酸和碳在加热的情况下反应的生成物,用图Ⅰ装置进行实验。

(1)请写出碳与浓硫酸反应的化学反应方程式_________________________________;该反应中氧化剂与还原剂的物质的量之比为_____________;
(2)图Ⅰ中A处是完成实验中的必要装置,它是下图所示中的_________;(填编号)
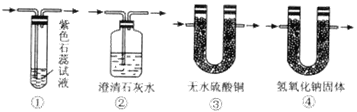
(3)图Ⅰ中C装置中应盛的试剂最好为:足够的_______________,其作用是__________________;
(4)若出现_______________________ 的实验现象,则可以确定存在二氧化碳气体。
(5)现实验小组的同学继续进行实验,他们将二氧化硫和氯气按一定的比例同时通入品红溶液中,一段时间后,发现品红溶液没有褪色。试分析实验过程中,品红不褪色的原因___________________(用离子反应方程式表示);你认为怎么样做可以让品红的颜色越来越浅?_________________。
【答案】 C+2H2SO4(浓) = 2SO2↑+CO2↑+2H2O 2:1 ③ KMnO4溶液 除去混合气体中的二氧化硫 C中高锰酸钾不褪色,D中澄清石灰水变浑浊 2H2O+SO2+Cl2 = 2Cl-+SO42-+4H+ 二氧化硫与氯气不以1:1通入
【解析】(1)浓硫酸有氧化性,加热时氧化性更强,木炭粉有还原性,两者相互反应,浓硫酸被还原成SO2,木炭粉则被氧化成CO2,反应生成SO2、CO2和H2O,反应的化学方程式是C+2H2SO4(浓) = 2SO2↑+CO2↑+2H2O;根据反应方程式可知,氧化剂H2SO4和还原剂的物质的量之比为2:1;(2)检验水蒸气的试剂是无水硫酸铜;若在通过水溶液后再检验则无法检验水是否是生成物,图Ⅰ中A处是完成水检验的实验,必要装置选③;(3)图Ⅰ中C装置是除去二氧化硫且检验二氧化硫已除尽,应盛的试剂最好为:足够的KMnO4溶液,其作用是除去混合气体中的二氧化硫;(4)若出现C中高锰酸钾不褪色,D中澄清石灰水变浑浊的实验现象,则可以确定存在二氧化碳气体;(5)若将二氧化硫和氯气按1:1同时通入品红溶液中,发生反应2H2O+SO2+Cl2 = 2Cl-+SO42-+4H+,则品红不褪色;若二氧化硫与氯气不以1:1通入,发生反应2H2O+SO2+Cl2 = 2Cl-+SO42-+4H+后剩余的SO2或Cl2均能使品红溶液褪色而颜色越来越浅。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
【题目】已知A~G有如图所示的转化关系(部分生成物已略去),其中A、G为单质,D是能使湿润的红色石蕊试纸变蓝色的气体,E、F均能与NaOH溶液反应.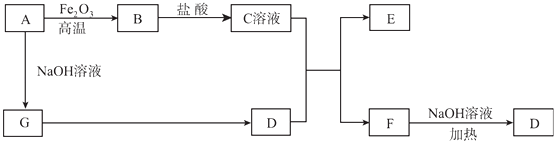
请回答下列问题:
(1)写出F的电子式:;
(2)①C溶液与D的水溶液反应的离子方程式为;②F溶液与NaOH溶液共热反应的化学方程式为;
(3)①请用离子方程式解释C溶液为何显酸性;②F溶液中离子浓度由大到小的顺序为;
(4)将5.4 g A投入到200 mL 2.0 mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是(填代号);
A.HNO3溶液
B.H2SO4溶液
C.NaOH溶液
D.HCl溶液
(5)将1mol N2和3mol G及催化剂充入容积为2 L的某密闭容器中进行反应,已知该反应为放热反应.平衡时,测得D的物质的量浓度为a mol/L.在其他条件不变的情况下,若起始时充入0.5 mol N2和1.5mol G达到平衡后,D的物质的量浓度(填“大于”“小于”或“等于”)a/2mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用20 mL 18.4 mol/L浓H2SO4和铜共热一段时间后,使反应混合物冷却,滤去多余的铜,将滤液加水定容到100 mL,测得SO42-离子物质的量浓度为3. 18 mol/L。试求溶液中CuSO4的物质的量浓度( )
A. 0.50 mol/L B. 0.75 mol/L C. 1.00 mol/L D. 3.18 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Fe(NO3)3和Cu(NO3)2的混合液中逐渐加入铁粉,溶液中Fe2+的物质的量浓度和加入铁粉的物质的量之间关系如图所示,则该溶液中Fe(NO3)3与Cu(NO3)2的物质的量浓度之比为
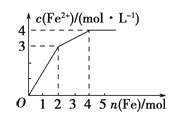
A.3∶1 B.1∶2 C.2∶1 D.1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式RO3n-+F2+mOH-=RO4- +aF- +H2O,试推算未知数n=___,a=___,m=____,RO3n- 中元素R的化合价为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色混合气体可能由CH4、H2、CO、CO2和HCl中的某几种气体组成。在恒温恒压条件下,通过过量的澄清石灰水未见变浑浊,但混合气体的总体积减小;把剩余气体导出后,在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体的成份是
A. HCl和CO B. HCl、H2和CO C. CH4和NH3 D. HCl、CO和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A.1 L0.6molL﹣1的食盐水中含氯化钠0.6mol
B.0.5mol碳酸钠溶于水配成0.5L溶液,所得溶液的物质的量浓度为0.5molL﹣1
C.标准状况下,44.8L氯化氢气体溶于1L水中所得溶液的物质的量浓度为2molL﹣1
D.20g氢氧化钠溶于水配成物质的量浓度为1molL﹣1的溶液,可得溶液1L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g)2HI(g)△H=﹣14.9kJ/mol.某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示.甲中反应达到平衡时,测得c(H2)=0.008mol/L. 下列判断正确的( )
起始浓度 | c(H2)/mol/L | c(I2)/mol/L | c(HI)/mol/L |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系的表述中,正确的是( )
A.0.1mol?L﹣1NaHSO4溶液中:c(Na+)+c(H+)=c(SO ![]() )+c(OH﹣)
)+c(OH﹣)
B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1
C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等
D.0.1mol?L﹣1NaHCO3溶液中:c(Na+)>c(HCO ![]() )>c(CO
)>c(CO ![]() )>c(H2CO3)
)>c(H2CO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com