
【题目】某蓄电池放电、充电的反应式为:Fe+Ni2O3+3H2O ![]() Fe(OH)2+2Ni(OH)2 , 下列推断中正确的是( ) ①放电时,Fe为正极,Ni2O3为负极;
Fe(OH)2+2Ni(OH)2 , 下列推断中正确的是( ) ①放电时,Fe为正极,Ni2O3为负极;
②充电时,阴极上的电极反应式是:Fe(OH)2+2e﹣═Fe+2OH﹣;
③充电时,Ni(OH)2为阳极;④蓄电池的电极必须浸在某碱性溶液中.
A.①②③
B.①②④
C.①③④
D.②③④
【答案】D
【解析】解:①由放电时的反应可以得出铁做还原剂失去电子,Ni2O3做氧化剂得到电子,即正极为Ni2O3、负极为Fe,故①错误;
②充电可以看作是放电的逆过程,即阴极为原来的负极,所以电池放电时,负极反应为:Fe+2OH﹣﹣2e﹣=Fe(OH)2,所以电池充电过程时阴极反应为Fe(OH)2+2e﹣=Fe+2OH﹣,故②正确;
③充电时,阴极发生Fe(OH)2+2e﹣=Fe+2OH﹣,阳极发生2Ni(OH)2+2OH﹣﹣2e﹣=Ni2O3+3H2O,Ni(OH)2做阳极,故③正确.
④根据总反应Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,可以判断出铁镍蓄电池放电时Fe作负极,发生氧化反应,为还原剂,失电子生成Fe2+,碱性电解质中最终生成Fe(OH)2,所以电解质溶液是碱,故④正确;
故选D.
根据电池的总反应:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,可以判断出铁镍蓄电池放电时Fe作负极,发生氧化反应,为还原剂,失电子生成Fe2+,最终生成Fe(OH)2,Ni2O3作正极,发生还原反应,为氧化剂,得电子,最终生成Ni(OH)2,电池放电时,负极反应为Fe+2OH﹣﹣2e﹣=Fe(OH)2,则充电时,阴极发生Fe(OH)2+2e﹣=Fe+2OH﹣,阴极附近溶液的pH升高,电池充电时,阳极发生2Ni(OH)2+2OH﹣﹣2e﹣=Ni2O3+3H2O.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】a.某有机物A化学式为CxHyOz,15 gA完全燃烧生成22 gCO2和9 gH2O。试确定:
(1)该有机物的最简式______________;
(2)若A的相对分子质量为60且和Na2CO3混合有气体放出,A和醇能发生酯化反应,则A的结构简式为 _______________ ;
(3)若A的相对分子质量为60且是易挥发有水果香味的液体,能发生水解反应,则其结构简式为______________;
(4)若A分子结构中含有6个碳原子,具有多元醇和醛的性质,则其结构简式为_______。
b.有机物A、B、C、D在一定条件下有如图所示的转化关系:

请回答下列有关问题:
(1)写出B的分子式:____________________。
(2)分别写出反应①的反应方程式______________和②的反应方程式________________________
(3)③的反应类型为___________________________。
(4)两分子D在浓硫酸存在的条件下加热可以发生自身的酯化反应生成E或F,且E的相对分子质量比F的小,则E和F的结构简式分别为___________________、_________________。
(5)下列关于有机物A的说法正确的有__________________(填序号)。
a.含有氢氧根离子,具有碱性
b.能发生加聚反应
c.能使溴水褪色
d.在一定条件下能与冰醋酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡.试回答: 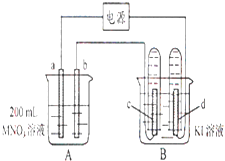
(1)a为极,d极的电极反应式为: .
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现象是 . 电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为: .
(3)当d电极上收集到44.8ml气体(标准状况)时停止电解,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在选项条件下一定能大量共存的是( )
A.无色溶液:Na+、Cu2+、Cl、NO3-
B.酸性溶液:NH4+、Fe3+、HCO3、SO42-
C.遇酚酞变红的溶液:Na+、K+、SO42-、NO3-
D.碱性溶液:K+、Al3+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图。下列说法正确的是( )

A. 铁片发生还原反应而被腐蚀
B. 铁片腐蚀最严重区域应该是生锈最多的区域
C. 铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-===4OH-
D. 铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中有如下图所示的反应,看图按要求回答下列问题: 
(1)上图中,反应物:Ⅰ是 , Ⅱ是 .
(2)写出反应方程式:Ⅰ , Ⅱ .
(3)在Ⅱ图中,以0~10s内的平均反应速率计算,t=6s时,A的浓度是mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如下图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的 乙炔气体中往往含有少量的 H2S 气体,请按下列要求填空:

(1)实验室制乙炔的化学方程式是:_________________;为了得到较为平稳的乙炔气流, 装置 A 的分液漏斗中常用_____来代替水.
(2)装置 B 中CuSO4溶液的作用是_____.
(3)装置 D 中观察到的现象是_____
(4)若称取m g 电石,反应完全后,测得B处溴的CCl4溶液增重n g,则CaC2的纯度为_____(用m与n表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com