



| A. | ③⑤⑥⑦ | B. | ②③④⑥ | C. | ①④⑤ | D. | 全部正确 |
分析 ①类比二氧化碳的电子式进行判断;
②硝基的表示方法不规范;
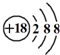
③氯离子的核电荷数为17,不是18;
④甲烷分子中含有4个碳氢键,为正四面体结构,碳原子半径大于氢原子;
⑤实验室为分子组成的最简比,又名最简式,根据葡萄糖的分子组成判断;
⑥元素符号的左上角为质量数,该氯原子的质量数应该为37;
⑦碳酸氢根离子水解生成碳酸和氢氧根离子,题中表示的碳酸氢根离子的电离方程式.
解答 解:①CSO分子中存在碳氧双键和碳硫双键,其电子式为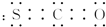 ,故①正确;
,故①正确;
②对硝基苯酚的结构简式中,硝基表示错误,正确的结构简式为: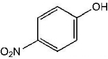 ,故②错误;
,故②错误;
③氯离子核电荷数为17,核外电子数为18,Cl-的结构示意图为: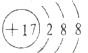 ,故③错误;
,故③错误;
④甲烷为正四面体结构,甲烷分子的比例模型为: ,故④正确;
,故④正确;
⑤葡萄糖的分子式为C6H12O6,则葡萄糖的实验式为:CH2O,故⑤正确;
⑥该氯原子的质量数为37,该氯元素可以表示为:1737Cl,故⑥错误;
⑦HCO3-的水解方程式为:HCO3-+H2O?H2CO3+OH-,故⑦错误;
故选C.
点评 本题考查了电子式、实验式、原子结构示意图等化学用语的判断,题目难度中等,试题的题量较大,涉及的知识点较多,注意掌握常见的化学用语的概念及正确的表示方法.


科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 用小苏打治疗胃酸过多:CO32-+H+=CO2↑+H2O | |
| D. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H+H→H-H | |
| B. | Mg+2HCl═MgCl2+H2↑ | |
| C. | 2Al+Fe2O3=Al2O3+2Fe | |
| D. | 2NH4Cl+Ba(OH)2•8H2O═BaCl2+2NH3↑+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
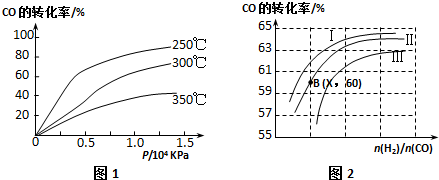
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将电能转化为化学能的过程 | |
| B. | 在过程②中若要获得无水MgCl2不可直接蒸干灼烧 | |
| C. | 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| D. | 第③④步的目的是为了浓缩富集溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、HCOOH、CH3COOC2H5.
、HCOOH、CH3COOC2H5.查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | X分子中有2个手性碳原子 | |
| B. | Y分子中所有原子可能在同一平面内 | |
| C. | 可用FeCl3溶液或NaHCO3溶液鉴别X和Y | |
| D. | 在NaOH溶液中,1 mol M最多可与4 mol NaOH发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com