
【题目】25℃时,向20.00mL0.1mol·L-1H2X溶液中滴入0.1mol·L-1 NaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-1gc水(OH-)]与所加NaOH溶液体积的关系如图所示。
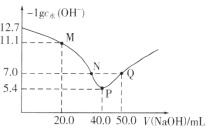
下列说法中正确的是
A. 水的电离程度:M>N=Q>P
B. 图中M、P、Q三点对应溶液中![]() 相等
相等
C. N点溶液中c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-)
D. P点溶液中c(OH-)=c(H+)+c(HX-)+c(H2X)
【答案】C
【解析】
A.M点:水电离出来的氢氧根离子为10-11.1mol/L,N点和Q点:水电离出来的氢氧根离子为10-7.0mol/L,P点水电离出来的氢氧根离子为10-5.4mol/L,水的电离程度:P>N=Q>M,故A错误;
B. H2X的第二步电离常数Ka2=![]() 得
得![]() =
=![]() ,电离常数只与温度有关为定值,在滴定过程中溶液中氢离子浓度一直在减小,因此M、P、Q三点对应溶液中氢离子浓度不等,
,电离常数只与温度有关为定值,在滴定过程中溶液中氢离子浓度一直在减小,因此M、P、Q三点对应溶液中氢离子浓度不等,![]() 不相等,故不选B;
不相等,故不选B;
C.N点为NaHX与Na2X的混合溶液,由图像可知,M点到P点发生HX-+OH-=H2O+X2-,根据横坐标消耗碱的量可知,在N点生成的X2-大于剩余的HX-,因此混合液n(Na2X)>n(NaHX),因为溶液呈中性,X2-的水解平衡与HX-的电离平衡相互抵消,所以N点溶液中c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-),故选C;
D. P点恰好生成Na2X溶液,根据质子守恒c(OH-)=c(H+)+c(HX-)+2c(H2X),故D错误;
答案:C


科目:高中化学 来源: 题型:
【题目】实验室需要0.3 mol/L NaOH溶液480 mL和1.0 mol/L硫酸溶液250 mL。根据这两种溶液的配制情况回答下列问题。
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。

(2)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.3 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.3 mol/L。
(3)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______mL(计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液存在![]() 、
、![]() 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值![]() 表示
表示 或
或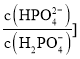 与pH的关系如图所示。已知碳酸
与pH的关系如图所示。已知碳酸![]() 、磷酸
、磷酸![]()
![]() 。则下列说法不正确的是( )
。则下列说法不正确的是( )
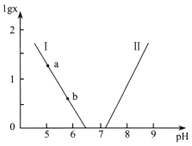
A.曲线Ⅱ表示 与pH的变化关系
与pH的变化关系
B.![]() 的过程中,水的电离程度逐渐增大
的过程中,水的电离程度逐渐增大
C.当![]()
![]() 时,
时,![]()
D.当pH增大时, 逐渐增大
逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的组成与结构决定了物质的性质与变化。请回答下列问题:
(1)钠元素的焰色反应呈黄色,其中黄色对应的辐射波长为______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)C、H、N、O四种元素中电负性最大的是______![]() 填元素符号
填元素符号![]() ,写出Fe2+的最外层电子排布式______。根据等电子原理,写出CN-的电子式______,CNO-中心原子的杂化方式为______。
,写出Fe2+的最外层电子排布式______。根据等电子原理,写出CN-的电子式______,CNO-中心原子的杂化方式为______。
(3)![]() 的沸点比
的沸点比![]() ______
______![]() 填“高”或“低”
填“高”或“低”![]() ;原因是______。
;原因是______。
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为______nm;MnO也属于NaCl型结构,晶胞参数为a’=0.448nm,则r(Mn2+)为______nm。
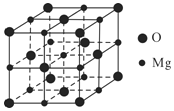
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各题。
(1)从下列物质中选择对应类型的物质的序号填空。
①CH3OCH3②HCOOCH2CH3③CH3COCH3④![]() ⑤CH3CHO⑥
⑤CH3CHO⑥![]() ⑦
⑦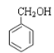
A.属于酯的是__;(填序号,下同)
B.属于酮的是__;
(2)下列各组物质:
①O2和O3;②乙醇和甲醚;③淀粉和纤维素;④苯和甲苯;⑤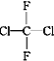 和
和![]()
![]() ;⑥
;⑥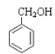 和
和![]() ;⑦CH3CH2NO2和
;⑦CH3CH2NO2和![]()
A.互为同系物的是__;(填序号,下同)
B.属于同一种物质的是__。
(3)为了测定芳香烃A的结构,做如下实验:
①将9.2g该芳香烃A完全燃烧,生成标况下15.68LCO2和7.2gH2O;
②用质谱仪测定其相对分子质量,得如图所示的质谱图,由图可知该分子的相对分子质量是__,有机物A的分子式为__。
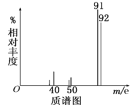
③用核磁共振仪处理该有机物得到四个峰,且四个峰的面积之比是1∶2∶2∶3,则该有机物A的结构简式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次递增的前四周期元素。A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满。据此回答下列问题。
(1)F元素形成的高价基态离子的核外电子排布式为__________。
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为__________。
(3)C、D、E元素的第一电离能由大到小的顺序是__________。(用元素符号表示)
(4)A和D形成的18电子化合物难溶于BE2,其理由是__________,此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为__________
(5)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________。
(6)F与C形成化合物的晶胞如图所示,该化合物的化学式为_____________,C离子的配位数是_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据酸碱质子理论判断,下列说法正确的是( )
A.由于水是中性的,故它既不是酸,也不是碱
B.![]() 可以被看作酸碱两性物质,与
可以被看作酸碱两性物质,与![]() 相似,
相似,![]() 也可以被看作酸碱两性物质
也可以被看作酸碱两性物质
C.![]() 溶液显酸性,
溶液显酸性,![]() 只能被看作酸
只能被看作酸
D.不但酸和碱可以用酸碱质子理论来分析,盐和水也可以用酸碱质子理论来分析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理饮食和正确使用药物能保证身心健康,这些都离不开化学。
(1)维生素是参与生物生长发育和新陈代谢所必需的一类小分子有机化合物;我们所熟悉的维生素有A、B、C、D、E等。其中维生素C又称___________________;其水溶液显______性,它能使酸性高锰酸钾溶液褪色,具有较强的_______性。
(2)某同学一天的食谱为:米饭、烙饼、豆腐、鸡蛋、糖醋排骨、酱牛肉。你认为这位同学还应该吃一些_________________食物,营养才算平衡。
(3)人们熟知的一种解热镇痛药阿司匹林的结构式为: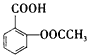 。请你写出其中含有的一种官能团的名称__________。阿司匹林属于____________(填有机物,无机物,氧化物)
。请你写出其中含有的一种官能团的名称__________。阿司匹林属于____________(填有机物,无机物,氧化物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)中药肉桂中含有有机物A,其球棍模型为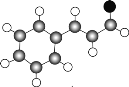 (分子中只含有C、H、O)。则有机物A的结构简式:____________,分子中含有的官能团名称是____________。
(分子中只含有C、H、O)。则有机物A的结构简式:____________,分子中含有的官能团名称是____________。
(2)按系统命名法给有机物 命名:_________________。
命名:_________________。
(3)a、苯酚;b苯甲醇;c、苯甲酸;d、碳酸 四种物质均含有羟基
①写出羟基的电子式___________;
②写出苯酚的电离方程式________________;
③上述4种物质酸性由强到弱的顺序为_______________(填字母)。
(4)写出下列反应的化学方程式
①乙炔与氢气用镍作催化剂在加热条件下反应生成乙烷_________________。
②甲苯制TNT_____________________。
③乳酸在一定条件下生成聚乳酸________________________。
④2分子甘氨酸脱去2分子水_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com