
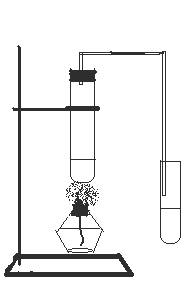
实验室用右图所示的装置制取乙酸乙酯。
(1)写出制取乙酸乙酯的化学方程式:
(2)装置中通蒸气的导管要插到饱和碳酸钠溶液液面上,而不能插入液面以下,目的是防止_________事故的发生。 收集了乙酸乙酯的试管振荡时有气泡产生,请解析产生气泡的原因(用化学方程式表示) 。
(3)实验制取的乙酸乙酯,可用 方法分离乙酸乙酯与饱和的碳酸钠溶液,请用用文字说明使用这种方法的理由: 。
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
.下列指定反应的离子方程式正确的是
A.用CH3COOH溶解CaCO3:CaCO3+2H+===Ca2++H2O+CO2↑
B.Cu溶于稀硝酸HNO3:Cu+2H++NO3-===Cu2++NO2↑+H2O
C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
D.向NaAlO2溶液中通入过量CO2:CO2+AlO2-+2H2O===Al(OH)3↓+HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为日常生活中常见的金属单质,其它均为化合物且B为红棕色固体。请回答下列问题:21世纪教育网版权所有
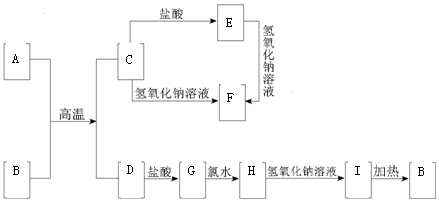 |
(1)写出A的原子结构示意图
(2)写出下列物质的化学式: B: E:
(3)写出下列反应的化学方程式或离子方程式:
C→F的化学方程式
G→H的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋面积占地球总面积的 。海洋中含有丰富的资源,海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
(1)写出镁元素在周期表中的位置:
(2)氯化钠的电子式 ,用电子式表示水的形成过程
(3)写出重水中的氢元素的核素符号:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子中,能在指定溶液中大量共存的是
A.澄清透明的溶液:ClO-、MnO4-、Al3+、SO42-
B.常温下c(H+)/c(OH-)=1012的溶液:Na+、SO42-、S2O32-、Cl-
C.无色溶液中:Cl–,I-,Na+,ClO-
D.含有大量AlO2-的溶液:CO32-、K+、SO42-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.氟化氢水溶液中存在的氢键有4种
B.H—O键键能为463 kJ·mol-1,即18 g 气态水分解成H2和O2时,消耗能量为2×463 kJ
C.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,观察现象可比较26Al、26Mg金属性强弱
D.室温下,V1 L pH=3的硫酸与V2LpH=11的NaOH溶液溶液混合,忽略分子间间隙引起的体积变化,若混合后溶液pH=4,则V1:V2=11:9
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示, 若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是

A.纯水中25℃时的c(H+)比100℃时的c(H+)大
B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3
C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1
D.25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
查看答案和解析>>
科目:高中化学 来源: 题型:
“分类”的思想方法,在化学发展中起到了重要作用.下列分类标准合理的是 ( )
A.只含一种元素的物质一定是单质
B.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
C.溶于水后能电离出H+的化合物都为酸
D.有单质生成的反应一定是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com