
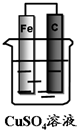
 如图装置能否形成原电池?若能,分别写出原电池的电极反应式.
如图装置能否形成原电池?若能,分别写出原电池的电极反应式. 分析 铁与硫酸铜溶液能够自发的氧化还原反应,所以铁是原电池的负极,碳提正极,负极的电极反应式为:Fe-2e-=Fe2+,正极的电极反应式为:Cu2++2e-=Cu,由此分析解答.
解答 解:(1)极为是铁,电极反应式为Fe-2e-=Fe2+,正极为铜,电极反应式为 Cu2++2e-=Cu,故答案为:铁;Fe-2e-=Fe2+;铜; Cu2++2e-=Cu;
(2)电子由负极铁经导线流向正极铜,若反应过程中有0.2mol电子发生转移生成0.1mol的铜,则生成的铜的质量为6.4g,故答案为:铁;铜;6.4g.
点评 本题考查学生原电池的工作原理,注意根据电极材料的活泼性判断正负极,根据正极上得失电子确定电极反应式的类型书写.


科目:高中化学 来源: 题型:选择题
| A. | I-Fe3+ Na+ | B. | Al3+Ba2+HCO3- | C. | K+Na+CO32- | D. | NH4+K+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,如果要合成
,如果要合成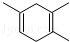 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 2,3-二甲基-1,3-丁二烯和1-丁炔 | B. | 2-甲基-1,3-丁二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2-甲基-1,3-丁二烯和丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
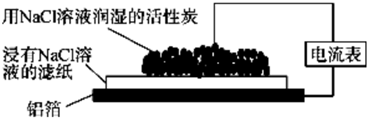
| A. | 该装置电流表中没有电流通过 | |
| B. | 铝箔是正极 | |
| C. | 总反应为4Al+3O2+6H2O═4Al(OH)3 | |
| D. | 电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
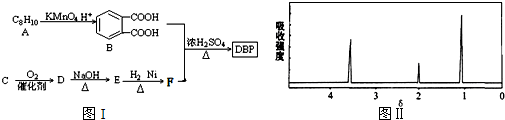
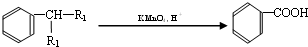
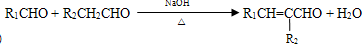 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基) ,该反应的反应类型为取代反应;
,该反应的反应类型为取代反应;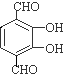 、
、 等
等查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com