
| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| B. | 碘水中通入足量的SO2:I2+SO2+2H2O═2I-+SO42-+4H+ | |
| C. | 用惰性电极电解饱和MgCl2溶液:2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+2OH-+Cl2↑ | |
| D. | NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
分析 A.发生氧化还原反应生成硫酸铁、NO、S和水;
B.发生氧化还原反应生成硫酸和HI;
C.电解生成氢氧化镁、氢气、氯气;
D.以2:1反应,生成硫酸钡、硫酸钠和水.
解答 解:A.硫化亚铁溶于稀硝酸中的离子反应为FeS+4H++NO3-=Fe3++S↓+NO↑+2H2O,故A错误;
B.碘水中通入足量的SO2的离子反应为I2+SO2+2H2O═2I-+SO42-+4H+,故B正确;
C.用惰性电极电解饱和MgCl2溶液Mg2++2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Mg(OH)2↓+Cl2↑,故C错误;
D.NaHSO4溶液与Ba(OH)2溶液反应至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电解反应、氧化还原反应的离子反应考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
| Ⅰ实验结果 | Ⅱ回答问题 |
| ①取原溶液少许,滴加足量氯水,产生沉淀;过滤,滤液加CCl4,振荡后,CCl4层未变色. | ①该步实验说明溶液中不存在Br-离子I-. |
| ②取原溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色. | ②该步实验发生反应的离子方程式为 8H++2NO3-(稀)+3Cu=3Cu2++2NO↑+4H2O. |
| ③取原溶液少许,加盐酸酸化后,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失. | ③产生白色沉淀的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+. |
| ④取原溶液少许,滴加2滴酸性高锰酸钾溶液,紫色立即褪去. | ④该步实验说明溶液中存在SO32-离子. |
| ⑤取原溶液少许,加足量Ba(NO3)2溶液产生白色沉淀,过滤;往洗涤后的沉淀中加入足量盐酸,沉淀部分溶解,有无色气体产生. | ⑤未溶解的白色沉淀是BaSO4;将气体通入品红溶液的现象是品红溶液褪色. |
| ⑥取步骤⑤所得滤液,加HNO3酸化后,再加AgNO3溶液,溶液中析出白色沉淀. | ⑥该步骤是否有意义有(填“有”或“无”). |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
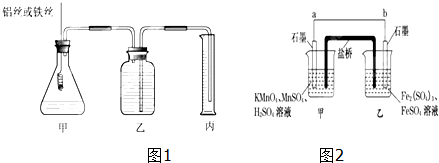
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯由于甲基对苯环的影响,导致苯环上甲基邻、对位上的氢原子易被取代而使溴水褪色 | |
| B. | 乙醇由于羟基的影响,导致乙醇甲基上的C-H键易断裂而发生消去反应生成乙烯 | |
| C. | 苯酚由于苯环的影响,导致酚羟基能与Na2CO3溶液反应生成CO2 | |
| D. | 苯酚由于羟基对苯环的影响,导致苯环上羟基邻、对位上的氢原子只能于液溴发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O (g)═H2(g)+$\frac{1}{2}$O2(g);△H=-485 kJ/mol | B. | H2O (g)═H2(g)+$\frac{1}{2}$O2(g);△H═+485 kJ/mol | ||
| C. | 2H2(g)+O2 (g)═2H2O(g)△H=+485 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(g)△H=-485 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应(1)和(2)均为氧化还原反应 | |
| B. | 反应(1)的氧化剂是O2,还原剂是FeO•Cr2O3 | |
| C. | 高温下,O2的氧化性大于Fe2O3小于Na2CrO4 | |
| D. | 生成1mol的Na2Cr2O7时共转移7mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 2.7g金属铝无论与强碱还是强酸作用时失去电子数目均为0.3NA | |
| C. | 22.4LN2分子中所含原子数为2 NA | |
| D. | 10.6g Na2CO3(Na2CO3 化学式量为106)固体含有的Na+离子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:
A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com