
A、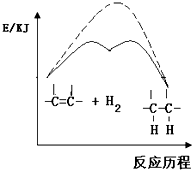 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下表示 |
B、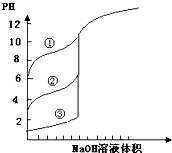 用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,曲线可确定①的酸性最强 |
C、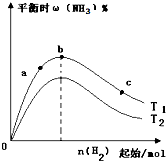 表示合成氨反应在其他条件不变的情况下,改变起始n(H2)对平衡的影响.由此可知,N2转化率最高的是b点;且T1>T2,K2>K1(T1和T2 表示温度,K1、K2表示对应温度下的平衡常数) |
D、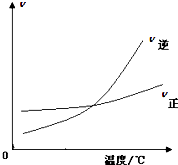 表示可逆反应“A2(g)+3B2 (g)?2AB3(g)”△H小于0 |


科目:高中化学 来源: 题型:
| A、它们所含的电子数目之比为1:1 |
| B、它们所含的O原子数目之比为1:2 |
| C、它们所含的C原子数目之比为1:1 |
| D、它们所含的原子总数目之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
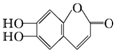 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是| A、M的相对分子质量是180 |
| B、M与足量的NaOH溶液发生反应消耗2molNaOH |
| C、1mol M与足量NaHCO3反应生成2mol CO2 |
| D、1mol M最多能与3mol Br2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、②④ |
| C、③④⑤ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴加酚酞试液显红色的溶液:Fe2+、NH4+、Cl-、I- |
| B、水电离出来的C (H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| C、在C (H+)=10-13mol/L的溶液:K+、SO42-、Al3+、Cl- |
| D、PH=1的溶液:Cu2+、Na+、Mg2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的PH值增大;碳酸钠溶液的水解程度减小 |
| B、Na+和CO32-的浓度都减小 |
| C、阴极与阳极析出的气体物质的量之比为1:2 |
| D、溶液的浓度不变,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com