
ŅŅ¶žĖįĖ×³Ę²ŻĖį£¬ĪŖ¶žŌŖĖį£Ø½į¹¹¼ņŹ½ĪŖHOOC£COOH£¬æɼņŠ“ĪŖH2C2O4£©”£25”ꏱ£¬²ŻĖįµÄµēĄėĘ½ŗā³£ŹżK1£½5.0”Į10£2£¬K2£½5.4”Į10£5£»Ģ¼ĖįµÄµēĄėĘ½ŗā³£ŹżK1£½4.5”Į10£7£¬K2£½4.7”Į10£11”£²ŻĖįøʵÄKsp£½4.0”Į10£8£¬Ģ¼ĖįøʵÄKsp£½2.5”Į10£9”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĖ®ČÜŅŗÖŠ²ŻĖįµÄµēĄė·½³ĢŹ½£ŗ ”£
£Ø2£©25”ę£¬ĪļÖŹµÄĮæÅØ¶Č¶¼ĪŖ0.1 mol/LµÄNa2C2O4ČÜŅŗµÄpH±ČNa2CO3ČÜŅŗpH______________________£ØĢī”°“ó”±”°Š””±»ņ”°ĻąµČ”±£©”£
£Ø3£©³£ĪĀĻĀ½«0.2 mol/LµÄKOHČÜŅŗ10 mLÓė0.2 mol/LµÄ²ŻĖįČÜŅŗ10 mL»ģŗĻ£¬Čō»ģŗĻČÜŅŗĻŌĖįŠŌ£¬ŌņøĆČÜŅŗÖŠĖłÓŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³Šņ£ŗ____________________”£
£Ø4£©25”ꏱĻņ20 mLĢ¼Ėįøʵı„ŗĶČÜŅŗÖŠÖšµĪ¼ÓČė1.0”Į10£3 mol/LµÄ²ŻĖį¼ŲČÜŅŗ20 mL£¬ÄÜ·ń²śÉś³Įµķ£æ________________£ØĢī”°ÄÜ”±»ņ”°·ń”±£©”£
£Ø5£©³żČ„¹ųĀÆĖ®¹øÖŠµÄCaSO4æÉĻČÓĆĢ¼ĖįÄĘČÜŅŗ“¦Ąķ£¬¶ųŗóÓĆŃĪĖįČܽā£¬Ęä·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ______________________________£»________________________________”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĶ¬Ń§ŌŚÓĆĻ”ĮņĖįÓėŠæÖĘČ”ĒāĘųµÄŹµŃéÖŠ,·¢ĻÖ¼ÓČėÉŁĮæĮņĖįĶČÜŅŗæɼÓæģĒāĘųµÄÉś³ÉĖŁĀŹ”£Ēė»Ų“šĻĀĮŠĪŹĢā:
(1) (2·Ö)ĮņĖįĶČÜŅŗæÉŅŌ¼ÓæģĒāĘųÉś³ÉĖŁĀŹµÄŌŅņ
ӣ
(2) (1·Ö)ŹµŃéŹŅÖŠĻÖÓŠNa2SO4”¢MgSO4”¢Ag2SO4”¢K2SO4µČ4ÖÖČÜŅŗ,æÉÓėÉĻŹöŹµŃéÖŠCuSO4ČÜŅŗĘšĻąĖĘ×÷ÓƵďĒ”” ”£
(4) (2·Ö)ŅŖ¼ÓæģÉĻŹöŹµŃéÖŠĘųĢå²śÉśµÄĖŁĀŹ,»¹æɲÉČ”µÄ“ėŹ©ÓŠ(“šĮ½ÖÖ)£ŗ
£»
”””£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆŅ»¶ØĮæµÄĢśÓė×ćĮæµÄĻ”H2SO4¼°×ćĮæµÄCuOÖʵ„ÖŹĶ£¬ÓŠČĖÉč¼ĘŅŌĻĀĮ½ÖÖ·½°ø£ŗ
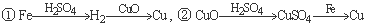
Čō°“ŹµŃéŌŌņ½ųŠŠ²Ł×÷£¬ŌņĮ½ÕßÖʵƵ„ÖŹĶµÄĮæµÄ±Č½ĻÕżČ·µÄŹĒ£Ø £©
A£®¢Ł¶ą B£®¢Ś¶ą C£®ĻąµČ D£® ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪŅ¹śÄ³“ó³ĒŹŠ½ńÄźĻļ¾¶ą“Ī½µĻĀĖįÓź”£¾Ż»·±£²æĆŲā¶Ø£¬øĆ³ĒŹŠÕūøöĻļ¾ĖįÓźµÄpHĘ½¾łĪŖ3.2£¬ŌŚÕāÖÖ»·¾³ÖŠµÄĢśÖĘĘ·¼«Ņ×±»øÆŹ“”£¶Ō“ĖĢõ¼žĻĀĢśµÄøÆŹ“µÄŠšŹö²»ÕżČ·µÄŹĒ£ŗ
| ”” | A£® | “ĖøÆŹ“¹ż³ĢÓŠ»ÆѧøÆŹ“Ņ²ÓŠµē»ÆѧøÆŹ“ |
| ”” | B£® | ·¢Éśµē»ÆѧøÆŹ“Ź±µÄÕż¼«·“Ó¦ĪŖ 2H2O+O2+4e©ØT 4OH© |
| ”” | C£® | ŌŚ»ÆѧøÆŹ“¹ż³ĢÖŠÓŠĒāĘų²śÉś |
| ”” | D£® | ·¢Éśµē»ÆѧøÆŹ“Ź±µÄøŗ¼«·“Ó¦ĪŖFe©2e©ØT Fe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijČÜŅŗÖŠ“óĮæ“ęŌŚČēĻĀĪåÖÖĄė×Ó£ŗNO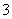 ”¢SO
”¢SO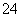 ”¢Fe3£«”¢H£«”¢M£¬ĖüĆĒµÄĪļÖŹµÄĮæÖ®±ČŅĄ“ĪĪŖn(NO
”¢Fe3£«”¢H£«”¢M£¬ĖüĆĒµÄĪļÖŹµÄĮæÖ®±ČŅĄ“ĪĪŖn(NO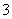 )”Ćn(SO
)”Ćn(SO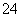 )”Ćn(Fe3£«)”Ćn(H£«)”Ćn(M)£½2”Ć3”Ć1”Ć3”Ć1£¬ŌņMæÉÄÜŹĒ£ŗ
)”Ćn(Fe3£«)”Ćn(H£«)”Ćn(M)£½2”Ć3”Ć1”Ć3”Ć1£¬ŌņMæÉÄÜŹĒ£ŗ
A£®Al3£«”””” B£®Mg2£« C£®CO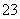 ”””” D£®Ba2£«
”””” D£®Ba2£«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖR2+Ąė×ÓŗĖĶāÓŠaøöµē×Ó£¬bøöÖŠ×Ó”£±ķŹ¾RŌ×Ó·ūŗÅÕżČ·µÄŹĒ
A£®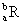 B£®
B£®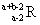 C£®
C£®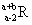 D£®
D£®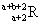
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°Ń¼×”¢ŅŅ”¢±ū”¢¶”ĖÄæ齚ŹōÅŻŌŚĻ”H2SO4ÖŠ£¬ÓƵ¼ĻßĮ½Į½ĻąĮ¬æÉŅŌ×é³Éø÷ÖÖŌµē³Ų”£Čō¼×”¢ŅŅĻąĮ¬£¬¼×µÄÖŹĮæ¼õÉŁ£»±ū”¢¶”ĻąĮ¬£¬¶”ÉĻÓŠĘųÅŻŅŻ³ö£»¼×”¢±ūĻąĮ¬£¬¼×ÉĻ·¢ÉśŃõ»Æ·“Ó¦£»ŅŅ”¢¶”ĻąĮ¬£¬ŅŅŹĒµē×ÓĮ÷ČėµÄŅ»¼«”£ŌņĖÄÖÖ½šŹōµÄ»īĘĆŠŌĖ³ŠņÓɓ󵽊”ÅÅĮŠĪŖ
A£® ¼×>ŅŅ>±ū>¶” B£® ¼×>±ū>ŅŅ>¶”
C£® ¼×>±ū>¶”>ŅŅ D£® ŅŅ>¶”>±ū>¼×
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö,Ēė²ĪÕÕŌŖĖŲ¢Ł”«¢ąŌŚ±ķÖŠµÄĪ»ÖĆ,ÓĆ»ÆѧÓĆÓļ»Ų“šĻĀĮŠĪŹĢā£ŗ
| ×å ÖÜĘŚ | IA | 0 | ||||||
| 1 | ¢Ł | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | |
| 2 | ¢Ś | ¢Ū | ¢Ü | |||||
| 3 | ¢Ż | ¢Ž | ¢ß | ¢ą |
£Ø1£©ÉĻŹö°ĖÖÖŌŖĖŲÖŠ£¬×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ £¬£ØĢī»Æѧ·ūŗÅ£¬ĻĀĶ¬£©£¬×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļ¼īŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ £¬×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļĻŌĮ½ŠŌµÄĒāŃõ»ÆĪļµÄ»ÆѧŹ½ŹĒ ”£
£Ø2£©¢ŪÓė¢ÜµÄĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌÓɓ󵽊”µÄĖ³ŠņŹĒ ”£
£Ø3£©¢Ü”¢¢Ż”¢¢ŽµÄĄė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ__________________”£
£Ø4£©¢Ś”¢¢Ū”¢¢ßµÄ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ______________”£
£Ø5£©¢Ł”¢¢Ü”¢¢Ż”¢¢ąÖŠµÄijŠ©ŌŖĖŲæÉŠĪ³É¼Čŗ¬Ąė×Ó¼üÓÖŗ¬¼«ŠŌ¹²¼Ū¼üµÄ»ÆŗĻĪļ£¬Š“³öĘäÖŠŅ»ÖÖ»ÆŗĻĪļµÄµē×ÓŹ½£ŗ______________”£
£Ø6£©ÓɱķÖŠŌŖĖŲŠĪ³ÉµÄ³£¼ūĪļÖŹX”¢Y”¢Z”¢M”¢NæÉ·¢ÉśŅŌĻĀ·“Ó¦£ŗ
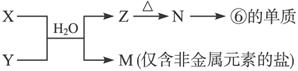
XČÜŅŗÓėYČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
×ćĮæĶÓėŅ»¶ØĮæÅØĻõĖį·“Ó¦£¬µĆµ½ĻõĖįĶČÜŅŗŗĶNO2”¢N2O4”¢NOµÄ»ģŗĻĘųĢ壬ÕāŠ©ĘųĢåÓė1.68 L O2(±ź×¼×“æö)»ģŗĻŗóĶØČėĖ®ÖŠ£¬ĖłÓŠĘųĢåĶźČ«±»Ė®ĪüŹÕÉś³ÉĻõĖį”£ČōĻņĖłµĆĻõĖįĶČÜŅŗÖŠ¼ÓČė6 mol”¤L-1NaOHČÜŅŗÖĮCu2+Ē”ŗĆĶźČ«³Įµķ£¬ŌņĻūŗÄNaOHČÜŅŗµÄĢå»żŹĒ A.60
mL B.45 mL C.30 mL D.50 mL
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com