
二氧化锰与浓盐酸混合加热得到氯气,如图是制取并探究Cl2化学性质的装置图。
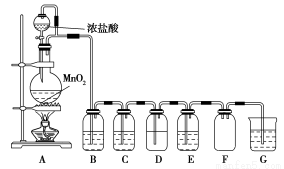
(1)圆底烧瓶中发生反应的化学方程式为 。
(2)若要得到干燥纯净的气体,B、C中应分别盛放的试剂为 、 。
(3)E中若装有FeCl2溶液,反应的离子方程式为 ,E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(4)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象某化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸加热
d.MnO2与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ,实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
(1)MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)饱和食盐水 浓硫酸
(3)2Fe2++Cl2=2Fe3++2Cl-
溶液变蓝
(4)①探究c(Cl-)对反应的影响 探究c(H+)对反应的影响 ②c(H+)的大小
【解析】(1)MnO2与浓盐酸反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)用该方法制得的氯气中含有HCl和水蒸气,分别用饱和食盐水和浓硫酸除去。
(3)氯气与FeCl2溶液反应的离子方程式是:2Fe2++Cl2=2Fe3++2Cl-。氯气将KI氧化为单质碘,单质碘使淀粉变蓝色。
(4)对比a、b、c、d、e五个实验方案可以看出,五个实验中都有MnO2和Cl-,只有a、c、e中有较高浓度的H+,这三个实验产生了Cl2,b、d中有较高浓度的Cl-,但无H+,没有产生Cl2,说明影响氯气生成的原因是H+浓度的大小。实验b的目的是探究c(Cl-)对反应的影响,实验c的目的是探究c(H+)对反应的影响。


 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:2014年高考化学一轮复习课后规范训练6-1练习卷(解析版) 题型:选择题
下列说法错误的是( )
A.化学反应中的能量变化都表现为热量变化
B.需要加热才能发生的反应不一定是吸热反应
C.向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的
D.反应物和生成物所具有的总能量决定了反应是放热还是吸热
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-1练习卷(解析版) 题型:选择题
锎是锕系中的一种元素,1 mg锎(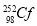 )每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是( )
)每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是( )
A.锎位于元素周期表第6周期
B.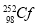 和
和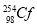 互为同位素
互为同位素
C.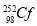 中,质子数和电子数均为98
中,质子数和电子数均为98
D.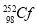 的中子数与质子数之差为56
的中子数与质子数之差为56
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-3练习卷(解析版) 题型:填空题
现有四个无标签的试剂瓶,分别盛有硫酸、BaCl2溶液、盐酸和不知名称的某正盐溶液M,将四种试剂分别标为A、B、C、D,取少量试剂分别进行实验得到如表格所示关系(其中无色气体能使澄清石灰水变浑浊,M溶液进行焰色反应为黄色)。
ABCD
A白色沉淀X白色沉淀Y
B白色沉淀X无色气体
(1)写出试剂名称:A ,B 。
(2)写出生成X的离子方程式: 。
(3)有人认为M是Na2CO3,此结论是否正确 (填“正确”或“不正确”),如认为正确,请说明推断的依据 ,如不正确,请说明理由 。
(4)若A、硝酸、D三种溶液混合后仍有沉淀,则其反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-3练习卷(解析版) 题型:选择题
下列叙述正确的是( )
A.含1 mol H2SO4的浓硫酸中有n(H+)=2n(SO42-)=2 mol
B.含1 mol H2SO4的浓硫酸和足量的锌完全反应,转移的电子为2 mol
C.配制2.0 mol·L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确)
D.用铜电极电解2.0 mol·L-1的硫酸,阴阳两极生成气体的体积之比为2∶1
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-2练习卷(解析版) 题型:选择题
氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-2练习卷(解析版) 题型:选择题
下列有关说法不正确的是( )
A.氯气通入淀粉碘化钾溶液中,溶液变蓝,氧化性:Cl2>I2
B.久置的氯水最终变为稀盐酸
C.明矾和漂白粉常用于自来水的处理,两者的作用原理不同
D.无色溶液C中加入AgNO3溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则无色溶液C中一定含有Cl-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-4练习卷(解析版) 题型:选择题
已知常温下D、E、F、H、L、N均为气体;A的焰色反应呈黄色;向B的溶液中滴加KSCN溶液,无明显现象;1 mol B隔绝空气分解得到F、G、H三种氧化物,其物质的量均为1 mol;F是易与血红蛋白结合的物质;J是现代社会中应用最广泛的金属单质。
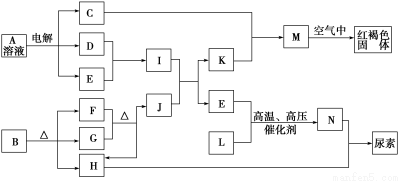
请回答下列题:
(1)B的化学式为________;H的结构式为________
(2)电解A溶液的离子方程式为______________________________________
(3)D与E反应可制得一种重要的化工原料,其反应的现象是____________________________
(4)F与G反应的化学方程式为________________________________
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:填空题
向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图
所示。请回答下列问题:

(1)b点时M的组成成分为______________________。
(2)若要使b点生成的盐的质量变为8.4 g,则应继续向溶液中通入二氧化碳________L(标准状况下)。
(3)若向生成的7.16 g盐的溶液中加入一定量的某物质,充分反应后,减压低温蒸发得到纯净的碳酸钠固体(无结晶水)8.4 g。
①若只加入0.03 mol某物质,则加入的物质可以是________或________;
②若只加入0.06 mol某物质,则加入的物质可以是________、________或________。
(4)常温下,同浓度的碳酸钠溶液和碳酸氢钠溶液的pH
都大于7,二者中________的pH更大,理由是________________________;0.1 mol·L-1碳酸钠溶液中离子浓度的大小关系是________;向碳酸氢钠溶液中逐滴滴入氢氧化钡溶液,发生反应的离子方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com