
在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变小 B.平衡向正反应方向移动
C.D的体积分数变大 D.a > c+d
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20 mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2 cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________________;
(2)上述B步骤操作的目的是________________________________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是___________________________________________________________;
(4)判断到达滴定终点的实验现象是_______________________________;
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生反应2SO2(g) + O2(g)  2SO3(g) △H<0。右图是该反应化学反应速率随时间变化的图象,推断在t1时刻突然变化的条件可能是( )
2SO3(g) △H<0。右图是该反应化学反应速率随时间变化的图象,推断在t1时刻突然变化的条件可能是( )
A.催化剂失效 B.增大容器的体积
C.降低体系温度 D.减小生成物的浓度

查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=-Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=-Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H=-Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
反应C(s)+H2O(g) CO(g)+ H2(g)在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( )
A.增加CO的物质的量
B.将容器的体积缩小一半
C.保持体积不变,充入N2使体系压强增大
D.保持压强不变,充入N2使容器体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2L的密闭容器中加入4mol A和6mol B,发生如下反应:2A(g)+3B(g) 4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是( )
4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是( )
A、前10min反应的平均速率V(C)=0.10mol/L·min
B、反应达平衡时B的平衡浓度是1.5mol/L
C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L
D 、10min后向容器中加入A,重新平衡时A的转化率一定大于50%
查看答案和解析>>
科目:高中化学 来源: 题型:
简答:
在水溶液中,橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:
Cr2O72- + H2O 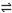 2CrO42- + 2H+ 把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
2CrO42- + 2H+ 把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
(1) 向上述溶液中加入NaOH溶液,溶液呈_________色,因为______________________
__________________________________________________________________。
(2) 向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈_________色,因为
_____________________ 。
(3) 向原溶液中逐滴加入Ba(NO3)2 溶液(已知BaCrO4为黄色沉淀),则平衡_______ ,溶液颜色将_______________ 。
(4)已知Cr2O72-与 I- 在酸性条件下可发生氧化还原反应:
Cr2O72--+ 16I- + 14 H+= 2Cr3++ 3 I 2+ 7 H2O
此反应中的氧化产物是_____,当消耗0.1 mol K2Cr2O7时,共有_________mol电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是-285.8 kJ·mol-1、-1411.0 kJ·mol-1和-1366.8 kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1
C.-330 kJ·mol-1 D.+330 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
现有金属单质A、B、C和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
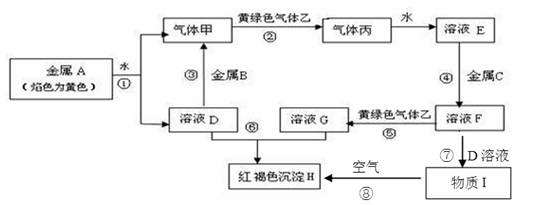
请根据以上信息回答下列问题:
(1)金属A的化学式为 ,气体乙的化学式为 金属C化学式为
(2)实验室检验G中所含的金属离子时,常在G的溶液中加入(填试剂名称) 溶液;
(3)反应④的离子方程式为 ;
(4)反应 的化学方程式为
的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com