
【题目】下列关于有机物的说法正确的是
A. 乙烷和新戊烷分子中所含甲基数之比为1∶1
B. 甲苯能发生加成反应、氧化反应和取代反应
C. 聚乙烯能使酸性KMnO4溶液和溴水褪色,但二者原理不同
D. ![]() 和C4H10的二氯代物的数目相同(不含立体异构)
和C4H10的二氯代物的数目相同(不含立体异构)
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
【题目】银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。将变黑的银质器皿放入下图装置,一段时间后发现黑色会褪去。回答下列问题:

(1)铝为______极,KNO3盐桥中的_______离子进入a烧杯中,银器的电极反应式为_________________________。
(2)如不用盐桥,将铝片和银器插入一个盛食盐水的烧杯中处理,阳极的电极反应式是_________,总反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨和铵盐的叙述正确的是
A. NH3易液化,常用作制冷剂
B. NH4Cl中含有少量的I2可通过加热的方法除去
C. 将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D. 某气体通入紫色石蕊试液后.溶液变红,据此可推断该气体为NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的中间产物,G的一种合成路线如下:

已知:
回答下列问题:
(1)A的结构简式是___________,E的化学名称是____________。
(2)由B生成C的化学方程式为______________________。
(3)G的结构简式为__________________。合成丁苯酞的最后一步转化为:
 ,则该转化的反应类型是_______________。
,则该转化的反应类型是_______________。
(4)有机物D的溴原子被羟基取代后的产物J有多种同分异构体,其中含有苯环的同分异构体有______种(不包括J),其核磁共振氢谱吸收峰最多的结构简式为_________。
(5)参照题中信息和所学知识,写出用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() 的合成路线:______________。
的合成路线:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将钠、镁、铝各0.3mol分别放入足量的盐酸中,同温同压下产生的气体的体积比是( )
A.1∶1∶1B.1∶2∶3C.6∶3∶2D.3∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:①氢氟酸;②浓H2SO4;③烧碱溶液;④Na2CO3固体;⑤氧化钙;⑥浓HNO3。其中在一定条件下能与SiO2反应的有( )
A. ①③④⑤ B. ②③⑥
C. ①②⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素和碳元素形成的单质及化合物在生产、生活中有广泛的用途,
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为_________________;其最外层电子的电子云形状为___________。
(2)(NH4)2Fe(SO4)2 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为____________________。
写出一种与NH4+互为等电子体的分子的电子式:________________________________。
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为______________。CO的沸点高于N2的原因是_________________________。
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为______________________。
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏加德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为________________;1cm3晶体的平均质量为___________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去);
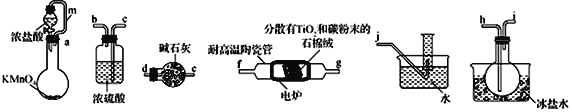
相关信息如下表所示:
熔点/℃ | 沸点/℃ | 密度/(g cm-3) | 水溶性 | |
TiCl4 | -25 | 136 | 1.5 | 易水解,能溶于有机溶剂 |
CC14 | -23 | 76.8 | 1.6 | 难溶于水 |
请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为_____________(填仪器接口字母)
(2)根据完整的实验装置进行实验,实验步骤如下:检査装置气密性后,装入药品;_____________
(按正确的顺序填入下列操作的字母)。
A.关闭分液漏斗活塞 B.停止加热,充分冷却
C.打开分液漏斗活塞 D.加热装置D中陶瓷管
实验时,当观察到______________时,开始进行步骤D。
(3)装置A中导管m的作用为_______________________。
(4)装置C的作用为 ___________________________________________。
(5)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为__________________________________。
(6)设计实验证明装置 F中收集到的液体中含有TiCl4:______________________________________________。
(7)制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如下图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是( )

A. 放电时电池总反应是4Na+3CO2 = 2Na2CO3+C
B. “吸入”CO2时的正极反应:4Na++3CO2+4e-=2Na2CO3+C
C. “呼出”CO2时钠箔电极反应式是Na++e-=Na
D. 每“呼出”22.4LCO2,转移电子数为4/3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com