
【化学-选修3:物质结构与性质】
X、Y、Z、R为前四周期原子序数依次增大的元素。X的单质与氢气可化合生成气体G.,其水溶液pH>7;Y的原子中最外层电子数是内层电子数的3倍;Z的单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。
请回答下列问题:
(1)Z元素在周期表中的位置________________;其单质的晶体类型是________________;X和Y元素的第一电离能较小的是___________(填元素名称);
(2)在Y、 Z的简单氢化物中,Y的氢化物更易溶于乙醇,其原因是_____________;G在一定条件下可与CO2反应生成一种最常见的氮肥M,M中所含元素原子的杂化方式为_____________;
(3) R单质与Z单质化合的产物J中,R离子的核外电子排布式是_____________;己知J与足量强碱性的NaC1O溶液在一定条件下反应,生成一种具有强氧化性的R的含氧酸根,该反应的离子方程式为_____________;
(4) G分子的立体构型为_______;R可形成化合物R(CO)5,该化合物中所含化学键的类型为_______;
(5) X与硼元素形成的化合物BX,其晶胞结构如图所示,该晶胞中含有的X原子数目为_____________;若最近的X、B原子之间的距离为anm,NA代表阿伏加德罗常数,则该晶体的密度为_____________g/cm
3(列式表示,不必化简)。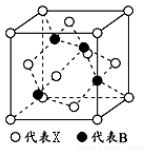
科目:高中化学 来源:2016届天津市和平区高三第二次模拟考试化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示。已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是( )。
X | ||||
Y | Z | W |
A.X分别与Y、Z形成的化合物中化学键类型相同
B.Z的最高价氧化物的对应水化物酸性比W的强
C.X的简单气态氢化物的稳定性比W的弱
D.Y是第三周期第ⅡA族元素
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:选择题
下列有机物在核磁共振氢谱上只给出一组峰的是
A .HCHO B .CH3OH C.HCOOH D.CH3COOCH3
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
下列说法正确的是

A.反应3NO2(g)+H2O(l)=2HNO3(l)+NO(g)在窒温下可自发进行,则该反应的△H<0
B.在铜的电解精炼过程中,若转移1mol电子,则阳极溶解32gCu
C.常温下向CuS的悬浊液中加入饱和MnSO4溶液可生成MnS沉淀,则Ksp(MnS))<Ksp(CuS)
D.常温下用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线(如右图)表示的是滴定盐酸的曲线
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
工业上常利用铝粉和氧化铁反应来焊接铁轨。下列说法正确的是
A.氧化铝、氧化铁均为两性氧化物
B.氧化铝中的微粒半径:r(Al3+)>r(O2-)
C.在该反应中,铝的还原性强于铁的还原性
D.1mol 氧化铁参加反应转移电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6,下列说法正确的是
A.原子半径大小的顺序为Z>X>Y>W
B.Y、Z两元素形成的简单阴离子的还原性Z>Y
C.X与W形成的化合物W2X2,含有离子键和共价键
D.Y、Z两种元素最高价氧化物的对应水化物的酸性Z>Y
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:实验题
化工原料红矾钠(重铬酸钠:Na2Cr2O7•2H2O)主要是以铬铁矿(主要成份为 FeO•Cr2O3,还含有A12O3、SiO2 等杂质)为主要原料生产,其主要工艺流程如下:
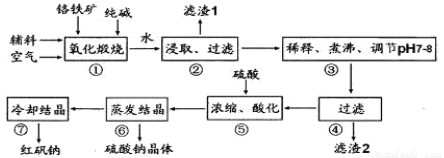
步骤①中主要反应的化学方程式为:4FeO•Cr2O3+8Na2CO3+7O2 =8Na2CrO4+2Fe2O3+8CO2
(1)杂质 A12O3、SiO2在①中转化后经加水过滤进入滤液,写出 A12O3在①中转化的化学反应方程式____________________________________。
(2)用化学平衡移动原理说明③中煮沸的作用是____________(用离子方程式结合文字说明)
(3)⑤中酸化是使 CrO42一转化为 Cr2O72一,若1L酸化后所得溶液中含铬元素的质量为 28.6 g,CrO42-有 转化为 Cr2O72-。
转化为 Cr2O72-。
①酸化后所得溶液中 c(Cr2O72- )=________
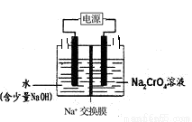
②工业上也可设计图示装置(两极均为惰性电极)电解Na2CrO4溶液制取 Na2Cr2O7,图中右侧电极的电极反应式为_________________________。若电解前两侧溶液的质量相等,则当电解过程中转移了1mol 电子时两侧溶液的质量差为______________g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
已知一定条件下体积不变的密闭容器中(各物质均为气态),1 mol N2和3 mol H2充分反应生成 NH3放热为Q1 kJ,下列说法正确的是
A.上述反应的热化学方程式为:N2(g)+3H2(g)  2NH3(g) ΔH=- Q 1 kJ/mol
2NH3(g) ΔH=- Q 1 kJ/mol
B.相同条件下1 mol N2 (g)和 3 mol H2(g) 的总键能小于2molNH3(g)的总键能
C.相同条件下将2 molN2 和6molH2置于相同容器中充分反应后放出的热量为 Q 2 kJ,Q2 =2Q1
D.相同条件下气体密度不变时,可以判断反应 N2(g)+3H2 (g) 2NH3 (g)达到平衡状态
2NH3 (g)达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A.向蛋白质溶液中滴加饱和Na2SO4溶液或浓硝酸均会产生白色沉淀,是因为蛋白质变性
B.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法
C.某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水,石灰水变浑浊,该钾盐一定是K2CO3
D.进行K与水反应的实验操作:可在培养皿中放些水,然后取绿豆大小的钾,用滤纸吸干表面的煤油,投入培养皿中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com