
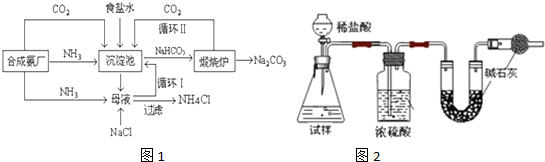
| 盐 | NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3?10H2O |
| 10℃ | 35.8 | 33.3 | 8.1 | 15.8 | 12.5 |
| 20℃ | 36.0 | 37.2 | 9.6 | 21 | 21.5 |


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
| A、体积都是22.4L |
| B、具有相同的体积 |
| C、具有相同的原子数 |
| D、具有相同的分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)+c(OH-)=c(A- )+c(H+) |
| B、c(Na+)=c(A-)+c(HA) |
| C、c(Na+)>c(OH-)>c(A-)>c(H+) |
| D、c(Na+)>c(A-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| SOCI2 |
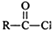
 +
+ →
→ +HCI
+HCI 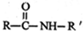
| NaOH溶液 |

查看答案和解析>>
科目:高中化学 来源: 题型:
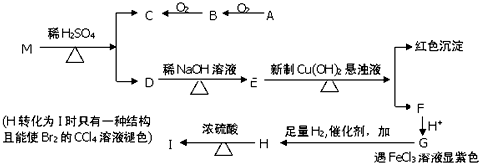
查看答案和解析>>
科目:高中化学 来源: 题型:
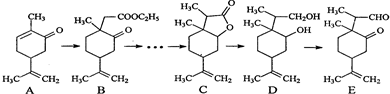
| LiBH4 |
| THF |
| LiBH4 |
| THF |
| CH3I |
| 催化剂 |
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硝酸 |
| 一定量NaOH |
| D的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
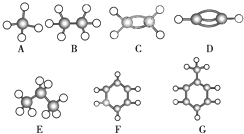 A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
A~G是几种烃的分子球棍模型(如图),据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | L层上有2对未成对电子 |
| X | 最外层电子数是次外层电子数的3倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com