
取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为()
A. 2.8mol•L﹣1 B. 3.2mol•L﹣1 C. 3.6mol•L﹣1 D. 无法判断
考点: 化学方程式的有关计算.
专题: 计算题.
分析: 将Cu2O拆分为Cu、CuO,原混合物看做Cu、CuO的混合物,其中一份用足量的氢气还原,反应后固体质量减少6.40g为拆分后Cu、CuO的混合物中O元素的质量,O原子的物质的量为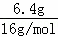 =0.4mol,根据Cu元素守恒可知n(CuO)=n(O)=0.4mol;另一份中加入500mL稀硝酸,固体恰好完全溶解,溶液中溶质为Cu(NO3)2,且同时收集到标准状况下NO气体4.48L,NO的物质的量为
=0.4mol,根据Cu元素守恒可知n(CuO)=n(O)=0.4mol;另一份中加入500mL稀硝酸,固体恰好完全溶解,溶液中溶质为Cu(NO3)2,且同时收集到标准状况下NO气体4.48L,NO的物质的量为 =0.2mol,根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=3n(NO),由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu),根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2],据此计算n(HNO3),再根据c=
=0.2mol,根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=3n(NO),由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu),根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2],据此计算n(HNO3),再根据c=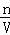 计算硝酸的浓度.
计算硝酸的浓度.
解答: 解:将Cu2O拆分为Cu、CuO,原混合物看做Cu、CuO的混合物,其中一份用足量的氢气还原,反应后固体质量减少6.40g为拆分后Cu、CuO的混合物中O元素的质量,O原子的物质的量为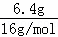 =0.4mol,根据Cu元素守恒可知n(CuO)=n(O)=0.4mol;
=0.4mol,根据Cu元素守恒可知n(CuO)=n(O)=0.4mol;
另一份中加入500mL稀硝酸,固体恰好完全溶解,溶液中溶质为Cu(NO3)2,且同时收集到标准状况下NO气体4.48L,NO的物质的量为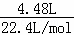 =0.2mol,根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=3n(NO)=3×0.2mol,n(Cu)=0.3mol,由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu)=0.4mol+0.3mol=0.7mol,根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2]=0.2mol+2×0.7mol=1.6mol,硝酸的浓度为
=0.2mol,根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=3n(NO)=3×0.2mol,n(Cu)=0.3mol,由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu)=0.4mol+0.3mol=0.7mol,根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2]=0.2mol+2×0.7mol=1.6mol,硝酸的浓度为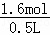 =3.2mol/L.
=3.2mol/L.
故选B.
点评: 本题考查混合物的计算、守恒计算等,难度中等,清楚反应过程是解题的关键,本题采取拆分法解答,简化计算过程,注意体会,可以通过列方程解答.


科目:高中化学 来源: 题型:
同温同压下,xg的甲气体和yg的乙气体占有相同的体积,根据阿伏加德罗定律判断,下列叙述错误的是()
A. x:y等于甲与乙的相对分子质量之比
B. x:y等于等质量的甲与乙的分子个数之比
C. x:y等于同温同压下甲与乙的密度之比
D. y:x等于同温同体积下等质量的甲与乙的压强之比
查看答案和解析>>
科目:高中化学 来源: 题型:
下列曲线图与对应选项不正确的是()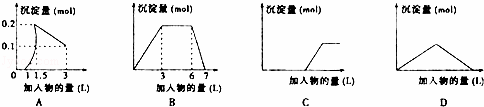
A. 向1L浓度均为0.1mol•L﹣1的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol•L﹣1稀H2SO4溶液
B. 向含有0.1 mol•L﹣1 AlCl3和0.3mol/L NH4Cl的1L混合液中逐滴加入0.1 mol•L﹣1NaOH溶液
C. 向烧碱溶液中逐滴加入明矾溶液
D. 向Ba(OH)2溶液中逐渐通入二氧化碳气体
查看答案和解析>>
科目:高中化学 来源: 题型:
化学工业是国民经济的支柱产业.下列生产过程中不涉及化学变化的是( )
A. 氮肥厂用氢气和氮气合成氨 B. 钢铁厂用热还原法冶炼铁
C. 硫酸厂用接触法生产硫酸 D. 炼油厂用分馏法生产汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250mL 0.10mol/L的NaOH溶液时,下列实验操作会使配得的溶液浓度偏小的是( )
A. 转移溶液后未洗涤烧杯和玻璃棒就直接定容
B. 在容量瓶中进行定容时仰视刻度线
C. 在容量瓶中定容时俯视刻度线
D. 定容后把容量瓶倒转摇匀,发现液面低于刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里做钠跟水反应的实验时,用到的仪器和药品是( )
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤研钵 ⑥烧杯 ⑦坩埚 ⑧石棉网 ⑨玻璃片 ⑩药匙.
A. ①②③④ B. ②③④⑥⑨ C. ③④⑧⑨⑩ D. ②⑤⑦⑨⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com