
【题目】CaCO3的摩尔质量为100g/mol,将5.0g CaCO3固体完全溶于稀盐酸后,再用蒸馏水稀释成100mL溶液.该溶液中Ca2+ 的物质的量浓度为( )
A.5.0 mol/L
B.0.50 mol/L
C.1.0 mol/L
D.0.10 mol/L
科目:高中化学 来源: 题型:
【题目】将一固体粉末含有SiO2、Fe2O3、Al2O3 , 加入足量NaOH溶液充分反应后,过滤,向所得溶液中加入过量盐酸,过滤,将所得滤渣洗涤并灼烧至恒重,最终固体成份为( )
A.SiO2
B.Fe2O3、SiO2
C.SiO2、Al2O3
D.Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.84gcm﹣3 , 溶质的质量分数为98%的硫酸,配制250mL物质的量浓度为0.46molL﹣1的硫酸.
(1)98%的浓硫酸的物质的量浓度为 .
(2)现有下列几种规格的量筒,应选用(用序号填空).
①5mL量筒 ②10mL量筒 ③50mL量筒 ④100mL量筒
(3)实验需要以下步骤:
①定容②量取③摇匀④洗涤⑤转移⑥冷却⑦计算⑧装瓶⑨稀释进行顺序为:
(4)下列操作使所配溶液的物质的量浓度偏高的是 .
A.往容量瓶中转移溶液时有少量液体溅出
B.未洗涤稀释浓H2SO4的小烧杯
C.定容时俯视刻度线
D.洗净容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪一项符合“绿色化学”的原则
A.排放前对废气、废水、废渣进行无害化处理
B.在化学生产中少用或不用有害物质以及少排放或不排放有害物质
C.在化工生产中,尽量避免使用任何化学物质
D.在化工厂范围多种草种树,努力构建花园式工厂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属性质的叙述中正确的是
A.钠与氧气反应时,产物是由O2的用量决定的
B.铝箔在空气中受热可以熔化且会发生剧烈燃烧
C.金属与非金属发生反应时,被氧化的一定是金属
D.铁丝不论在空气中还是在纯氧中都不会燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各电离方程式中,书写正确的是( )
A.CH3COOHH++CH3COO﹣
B.KHSO4K++H++SO42﹣
C.Al(OH)3Al3++3OH﹣
D.NaH2PO4Na++H2PO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于基本营养物质的说法错误的是( )
A. 淀粉和纤维素水解的最终产物均为葡萄糖
B. 在加热条件下,葡萄糖可与新制氢氧化铜浊液反应产生砖红色沉淀
C. 植物油含不饱和脂肪酸甘油酯,能使Br2的CCl4溶液褪色
D. 糖类、油脂和蛋白质均由C、H、O三种元素组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO47H2O广泛用于医药和工业领域.以下是FeSO47H2O的实验室制备流程图. 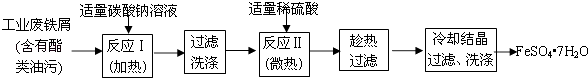
根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为(用离子方程式表示),
(2)废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答) , . 以下是测定某补血剂(FeSO47H2O)中铁元素含量的流程图.根据题意完成下列填空: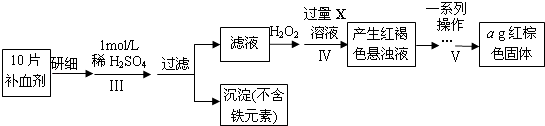
(3)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及 .
(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③④冷却⑤称量⑥恒重操作.操作⑥的目的是 .
(5)假设实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述错误的是( )
A. 植物油能使溴的四氯化碳溶液褪色
B. 淀粉水解的最终产物是葡萄糖
C. 葡萄糖能发生水解和氧化反应
D. 利用油脂在碱性条件下的水解,可以生产甘油和肥皂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com