
| 点燃 |
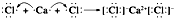 ,故答案为:
,故答案为: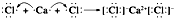 ;
;

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:

| 滴定序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为| 催化剂 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.
(1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.

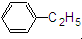

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Li2SO4难溶于水 |
| B、Li与水剧烈反应 |
| C、LiOH是易溶于水,受热不分解的强碱 |
| D、Li2CO3受热分解,生成Li2O和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H2SO3) | ||
c(HS
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤⑥ | B、②③④⑥ |
| C、②③④⑤ | D、①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com