
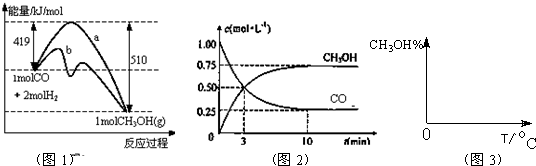
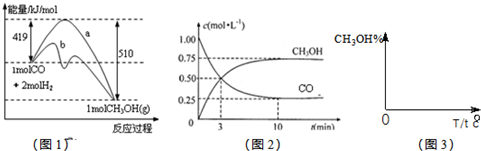
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)  CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4 mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4 mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
请回答下列问题:
(1)在“图1”中,曲线________(填:a或b)表示使用了催化剂;该反应属于________(填:吸热、放热)反应。
(2)下列说法正确的是________。
| A.起始充入的CO为1 mol |
| B.增加CO浓度,CO的转化率增大 |
| C.容器中压强恒定时,反应已达平衡状态 |
| D.保持温度和密闭容器容积不变,再充入1 mol CO和2 mol H2,再次达到平衡时n(CH3OH)/n(CO)会减小 |
 CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数________(填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数________(填“增大”、“减小”或“不变”)。 O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol(1)b(1分) 放热(1分) (2)C(1分)
(3)0.15 mol·L-1·min-1(2分) 12(2分) 减小(2分)
(4)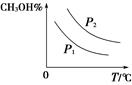 (2分)
(2分)
(5)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-280.9 kJ/mol(2分)
(6)6Co3++CH3OH+H2O=CO2↑+6 Co2++6H+(2分)
解析试题分析:(1)加入催化剂,能降低反应的活化能,故b曲线是加入了催化剂的;图中显示,反应物的总能量高于生成物的总能量,故该反应是放热反应;(2)容器体积为2L,故CO的加入量为2mol,A错;增加CO的浓度,其本身的转化率降低,B错;该反应前后气体分子总数不同,故当压强不变时,反应达到平衡状态;保持温度和密闭容器容积不变,再按1:2充入CO和H2,平衡右移,CO的转化率增大,故n(CH3OH)/n(CO)增大,D错;(3)CO的变化量为0.75 mol·L-1,故H2的变化量为1.5 mol·L-1;该反应的化学平衡常数为K= = =12;该反应为放热反应,温度升高,平衡左移,故平衡常数减小;(4)压强增大,平衡右移,甲醇的百分比增大;温度升高,平衡左移,甲醇的百分比降低;(5)32 g的CH3OH(g)为1mol,①-2②可得。
考点:化学平衡
点评:化学平衡是历年高考重中之重,考生一定要系统备考此知识点,同时配以练习,掌握必要解题思路。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| n(CH3OH) |
| n(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
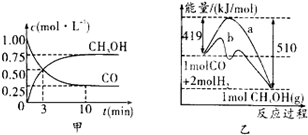
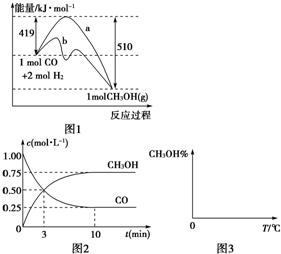 工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.| 3 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com