
| 5.6L |
| 22.4L/mol |
| n |
| V |
| 5.6L |
| 22.4L/mol |
| 3 |
| 2 |
|
|
| 0.5mol |
| 0.1L |
| 27g/mol×0.1mol |
| 5.1g |


科目:高中化学 来源: 题型:
| A、沸点:苯酚>甲醛>2一甲基丁烷 |
| B、2,2,3,3-四甲基丁烷、新戊烷、乙烷中化学环境相同的H原子种类由多到少 |
| C、密度:溴苯>H2O>苯 |
| D、等物质的量物质燃烧耗O2量:己烷>苯>C6H5COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3:2 | B、2:1 |
| C、9:2 | D、8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解时在阳极得到氯气,在阴极得到金属钠 |
| B、在阳极附近有黄绿色的气体产生 |
| C、在阴极附近的溶液中滴入酚酞溶液,溶液呈无色 |
| D、电解一段时间后,将电解液全部转移到烧杯中,充分搅拌后溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和C3H4,体积比为1:1 |
| B、C2H2和C2H6,体积比为3:1 |
| C、C2H4和C2H6,体积比为2:1 |
| D、C2H2 和C2H4,体积比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)>c(F-) |
| B、c(H+)>c(HF) |
| C、c(OH-)>c(HF) |
| D、c(HF)>c(F-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 装置 | 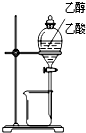 | 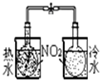 | 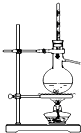 |  |
| 实验 | 分离乙醇和乙酸 | 证明温度对化学平衡的影响 | 分离沸点相差较大的互溶液体混合物 | 制取并收集氨气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
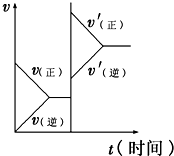 对于达到平衡的可逆反应:X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是( )
对于达到平衡的可逆反应:X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是( )| A、X、Y、Z、W均为气体 |
| B、Z、W为气体,X、Y中之一为气体 |
| C、X、Y、Z皆为气体,W为非气体 |
| D、X、Y为气体,Z、W中至少有一种为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
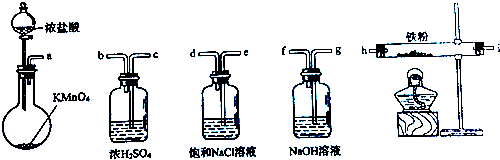
| A、a-b-c-d-e-e-f-g-h |
| B、a-e-d-c-b-h-i-g |
| C、a-d-e-c-b-h-i-g |
| D、a-c-b-d-e-h-i-f |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com